
| ||
| ||
| 4.5��0.8-2.4 |
| 0.8 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ﵽ��ѧƽ��ʱ���淴Ӧ��������Ҷ�Ϊ�� |
| B�������¶ȿ���߷�Ӧ���� |
| C��ʹ�ô�������������Ӧ���� |
| D������������Ũ�ȿ���߷�Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ�м�ˮϡ�ͺ���Һ�г���H2O����������Ũ�ȶ��½� |
| B��25��ʱ����10mL pH=a��������100mL pH=b��Ba��OH��2��Һ��Ϻ�ǡ���кͣ���a+b=13 |
| C�������ʵ���Ũ�ȵ�NaCl��Һ��CH3COONa��Һ�������ϣ�������Һ������Ũ�ȴ�С��ϵΪ��c��C1-����c��Na+����c��CH3COO-����c��OH-����c��H+�� |
| D������������ʵ���Ũ�ȵ�NaX������HX��Ϻ����Һ�Լ��ԣ�������Һ����Ũ�ȴ�С��ϵΪ��c��X-����c��Na+����c��HX����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ���� |

| ���¸�ѹ |
| ���� |
| �� �� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 3mol H2��2mol N2 | 6mol H2��4mol N2 | 2mol NH3 |
| �ﵽƽ���ʱ�䣨min�� | t | 5 | 8 |
| ƽ��ʱN2��Ũ�ȣ�mol?L-1�� | c1 | 3 | |
| N2��������� | ��1 | ��2 | ��3 |
| ��������ܶȣ�g?L-1�� | ��1 | ��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| ������kJ�� | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �۵� | �Ƿ���ȷ | �������� |
| ѧ��1 | �� | |
| ѧ��2 | ||
| ѧ��3 |
| �� |
| ��� |
| 2800�� |
| �� |
| C��� |
| 1352�� |
| �ٹ������� |
| �ڡ� |
| ��� |
| 714�� |
| ���� |
| ���ý��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
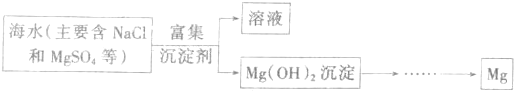
 �ɱ��ǹ�̬CO2���׳ƣ��������˹����꣬22g�ɱ���A��B��C��D����
�ɱ��ǹ�̬CO2���׳ƣ��������˹����꣬22g�ɱ���A��B��C��D�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�2.24L���������е�������ΪNA |
| B��1L1molmol?L-1�ռ���Һ������������ΪNA |
| C��1mol��������ˮ�γ���ˮ�Ĺ�����ת�Ƶĵ�����ΪNA |
| D�����³�ѹ�£�16gO2��O3���Ļ�������к��е���ԭ����ΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com