
| ʵ�鷽�� | ʵ�������� |
| ȡ�������������Թ��У���ˮ�ܽ�μ�����ϡ���� | ������ɫ������� |
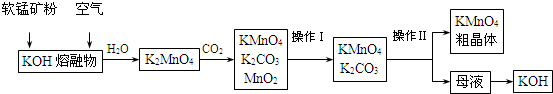
���� �������������������ڿ��������ڣ���ˮ�ܽ�õ�K2MnO4��Һ��ͨ�������̼�õ�KMnO4��MnO2��K2CO3�����˳�ȥ������MnO2������ҺΪKMnO4��K2CO3��Һ��Ũ���ᾧ�����ȹ��˵õ�KMnO4���壬ĸҺ�к���K2CO3����ĸҺ�м�ʯ���飨�������ƣ��õ�̼��Ƴ�����KOH��
��1���������̡�KOH�����������������·�Ӧ����K2 MnO4��H2 O��
��2������������ͼ���ܷ�Ӧ�����ɵ����ʿ�ѭ�����ã�̼����ܺ��������Ʒ�Ӧ����KOH��
��3����2MnO2+4KOH+O2 $\frac{\underline{\;����\;}}{\;}$2K2MnO4+2H2O ��֪�����ԭ����1mol MnO2ǡ�õõ�1mol K2MnO4����3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2֪��1mol K2MnO4�ڷ�Ӧ���ܵõ�$\frac{2}{3}$molKMnO4��
��4���������к��ж������裬���������ܺ�NaOH��Ӧ�������ƺ�ˮ�����������Թ������Һ���ù��˷�����
����KMnO4��K2CO3���ܽ����Ͻ��з��룻
��5��̼��غ�����ض�������ˮ����̼����ܺ�ϡ���ᷴӦ������ɫ���壬������غ�ϡ�����Ӧ�����Կ�����ϡ�������̼��أ�
��� �⣺�������������������ڿ��������ڣ���ˮ�ܽ�õ�K2MnO4��Һ��ͨ�������̼�õ�KMnO4��MnO2��K2CO3�����˳�ȥ������MnO2������ҺΪKMnO4��K2CO3��Һ��Ũ���ᾧ�����ȹ��˵õ�KMnO4���壬ĸҺ�к���K2CO3����ĸҺ�м�ʯ���飨�������ƣ��õ�̼��Ƴ�����KOH��
��1���������̡�KOH�����������������·�Ӧ����K2 MnO4��H2 O����Ӧ����ʽΪ2MnO2+4KOH+O2$\frac{\underline{\;����\;}}{\;}$2K2 MnO4+2H2 O���ʴ�Ϊ��2MnO2+4KOH+O2$\frac{\underline{\;����\;}}{\;}$2K2 MnO4+2H2 O��
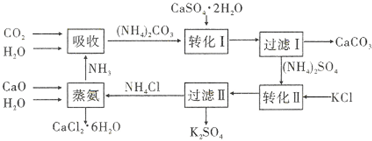
��2���Ʊ������õ�ԭ�ϣ���ת�������������ɵĿ���ѭ�����ã���ת����ϵͼ֪����ʯ�ҡ�������̼�⣬K2MnO4��Һ��ͨ��CO2���Ʊ�KMnO4���ɵ�MnO2�������ĸҺ����ʯ�����ɵ�KOH������MnO2��KOH�������Ʊ�K2MnO4�б�ѭ�����ã�
̼����ܺ��������Ʒ�Ӧ����KOH��������ĸҺ�Ƶ�KOHӦ�����������Ca��OH��2��
�ʴ�Ϊ��KOH��MnO2��Ca��OH��2��
��3����2MnO2+4KOH+O2 $\frac{\underline{\;����\;}}{\;}$2K2MnO4+2H2O ��֪�����ԭ����1mol MnO2ǡ�õõ�1mol K2MnO4����3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2֪��1mol K2MnO4�ڷ�Ӧ���ܵõ�$\frac{2}{3}$molKMnO4��
���Զ������̺����յõ�������صĹ�ϵʽ��3MnO2---2KMnO4��������Ҫ1.5molMn02�����Ƶ�1mol KMnO4���ʴ�Ϊ��1.5��
��4���������к��ж������裬���������ܺ�NaOH��Ӧ�������ƺ�ˮ����Ӧ����ʽΪSiO2+2NaOH�TNa2 SiO3+H2 O�����������Թ������Һ���ù��˷�������
����KMnO4��K2CO3���ܽ����Ͻ��з��룬Ȼ�������ᾧ�����ȹ��˵õ����壬
�ʴ�Ϊ��SiO2+2NaOH�TNa2 SiO3+H2 O�����ˣ��ܽ�ȣ������ᾧ��
��5��̼��غ�����ض�������ˮ����̼����ܺ�ϡ���ᷴӦ������ɫ���壬������غ�ϡ�����Ӧ�����Կ�����ϡ������飬����鷽����ȡ�������������Թ��У���ˮ�ܽ�μ�����ϡ���ᣬʵ�������dz�����ɫ���������֤������̼��ؾ��壬
�ʴ�Ϊ��ȡ�������������Թ��У���ˮ�ܽ�μ�����ϡ���������ɫ���������
���� ���⿼�������Ʊ����漰���ʼ��顢���ʷ�����ᴿ����ѧ����ʽ���йؼ��㡢�������̷����ȣ���ȷԪ�ػ��������ʡ����ʷ����ᴿ�������ǽⱾ��ؼ���ע�⣨3���ⲻ�ܵ����ؼ�Mnԭ���غ�õ���MnO2��KMnO4����ϵʽ����5�������̼��ز�����ϡ���ᣬ��Ϊϡ�����ܱ����Ը��������Һ������


 ������ҵ����ν�����������ϵ�д�
������ҵ����ν�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | þ���������������ȷ�Ӧ | B�� | �кͷ�Ӧ�����ȷ�Ӧ | ||
| C�� | ���ȷ�Ӧ�������ȷ�Ӧ | D�� | ̼��Ʒֽ������ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȣ��棩 | 0 | 20 | 60 |
| K2SO4�ܽ������g�� | 7.4 | 11.1 | 18.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
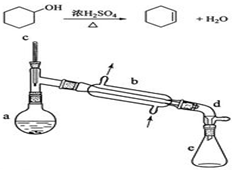 ����ˮ�Ǻϳ�ϩ���ij��÷�����ʵ���Һϳɻ���ϩ�ķ�Ӧ��ʵ��װ�����£�
����ˮ�Ǻϳ�ϩ���ij��÷�����ʵ���Һϳɻ���ϩ�ķ�Ӧ��ʵ��װ�����£�| ��Է������� | �ܶ�/��g•cm-3�� | �е�/�� | �ܽ��� | |
| ���Ѵ� | 100 | 0.9618 | 161 | ����ˮ |
| ����ϩ | 82 | 0.8102 | 83 | ������ˮ |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
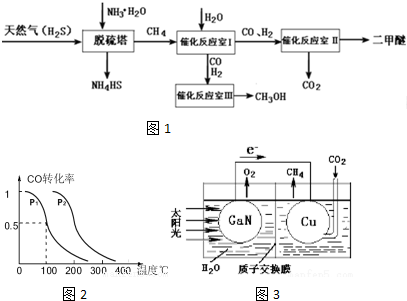
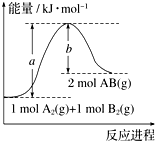 ͼ�����о���ѧ��Ӧ���ʱ��һ�ֳ��÷�������֪��ѧ��ӦA2��g��+B2��g���T2AB��g���������仯������ͼ��ʾ����������������ȷ���ǣ�������
ͼ�����о���ѧ��Ӧ���ʱ��һ�ֳ��÷�������֪��ѧ��ӦA2��g��+B2��g���T2AB��g���������仯������ͼ��ʾ����������������ȷ���ǣ�������| A�� | ÿ����2 mol ABʱ���գ�a-b�� kJ���� | |
| B�� | �÷�Ӧ�ȡ�H=+��a-b�� kJ•mol-1 | |
| C�� | �÷�Ӧ�з�Ӧ�������������������������� | |
| D�� | ����1 mol A-A��1 mol B-B��ʱ�ų�a kJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com