
 的分子式为:C8H18,其一氯代物有4种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:(CH3)3CC(CH3)3
的分子式为:C8H18,其一氯代物有4种,该烃有多种同分异构体,其中有一种一氯取代物只有一种,写出这种同分异构体的结构简式:(CH3)3CC(CH3)3 .
. 分析 (1)由于此有机物中较大的原子能形成4条价键,故为C原子;较小的原子只形成一条价键,故为氢原子,据此分析其分子式;根据其结构简式来分析其氢原子的种类,来得出其一氯代物的种类;其某同分异构体的一氯代物只有一种,说明其氢原子只有一种,结构非常对称,据此分析;
(2)根据减碳法作取代基,利用碳链异构书写C6H14的所有同分异构体;
(3)苯和浓硝酸在浓硫酸、加热条件下发生取代反应生成硝基苯.
解答 解:(1)由于此有机物中较大的原子能形成4条价键,故为C原子,此物质中共含8个碳原子;较小的原子只形成一条价键,故为氢原子,此物质中共含18个氢原子,故其分子式为:C8H18;
此有机物的结构简式为:(CH3)3CCH2CH(CH3)2,其中的氢原子有4种,故其一氯代物的种类有4种;
其同分异构体的一氯代物只有一种,说明其氢原子只有一种,结构非常对称,故其结构简式为:(CH3)3CC(CH3)3;故答案为:C8H18; 4;(CH3)3CC(CH3)3;
(2)C6H14属于烷烃,主链为4个碳原子有:CH3CH2C(CH3)3、CH3CH(CH3)CH(CH3)CH3,共有2种,故答案为:2;
(3)苯和浓硝酸在浓硫酸、加热条件下发生取代反应生成硝基,方程式为: ,
,
故答案为: .
.
点评 本题以苯为载体,考查了有机物的结构、性质及有机物同分异构体的书写,难度不大,推断有机物时要根据物质的性质及官能团进行分析.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:解答题
 2014年10月,北京、哈尔滨等多个北方城市出现严重雾霾天气,多所学校被迫停课,造成雾霾的“罪魁”之一是汽车尾气.当今汽车尾气处理主要经三元催化器处理,其主要污染物(CO、NOx,碳氢化合物)可自发的相互反应变成无害气体,减少环境污染,其反应原理之一:2NO(g)+2CO(g)═N2(g)+2CO(g)△H,回答下列问题:
2014年10月,北京、哈尔滨等多个北方城市出现严重雾霾天气,多所学校被迫停课,造成雾霾的“罪魁”之一是汽车尾气.当今汽车尾气处理主要经三元催化器处理,其主要污染物(CO、NOx,碳氢化合物)可自发的相互反应变成无害气体,减少环境污染,其反应原理之一:2NO(g)+2CO(g)═N2(g)+2CO(g)△H,回答下列问题:| 时间/s | 0 | 2 | 3 | 4 |
| C(NO0(×10-4mol•L-1) | 20.0 | 3.00 | 2.00 | 2.00 |
| C(CO)(×10-3mol•L-1) | 2.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HSO3-在溶液中发生水解:HSO3-+H2O?SO32-+H3O+ | |
| B. | 向NaClO溶液中通入少量SO2:2ClOˉ+SO2+H2O═SO32ˉ+2HClO | |
| C. | 苯酚钠溶液显碱性:C6H5O-+H2O?C6H5OH+OH- | |
| D. | 惰性电极电解MgCl2溶液:Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ OH-+Cl2↑+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电解质溶液中Cl-向a电极迁移 | |
| B. | 该装置能将化学能转变成电能 | |
| C. | b电极上发生氧化反应 | |
| D. | 若b为铁,则b电极的反应式为:Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醛的分子式:C2H4O | B. | 苯的结构简式: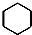 | ||
| C. | 乙炔的结构简式:CH≡CH | D. | 乙醇的结构简式:C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com