
分析 ①2C(S)+O2(g)=2CO(g)△H=-221kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1
根据盖斯定律可知:$\frac{①-②×2}{2}$得到热化学方程式为:C(S)+H2O(g)=CO(g)+H2(g)以此来计算.
解答 解:①2C(S)+O2(g)=2CO(g)△H=-221kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1
根据盖斯定律可知:$\frac{①-②×2}{2}$得到热化学方程式为:C(S)+H2O(g)=CO(g)+H2(g)△H=$\frac{-221+241.8×2}{2}$kJ/mol=+131.3kJ/mol;
即C(S)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol;
故答案为:C(S)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol.
点评 本题考查了热化学方程式的应用,盖斯定律的应用,焓变的含义,热化学方程式的推导过程中注意焓变的计算.


科目:高中化学 来源: 题型:实验题
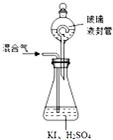 二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题:
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题: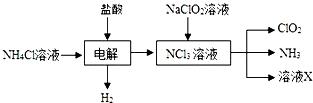
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| B. | SiO2(s)+2C(s)=Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0 | |
| C. | 常温下,NH4Cl溶液加水稀释,$\frac{{c(N{H_3}•{H_2}O)•c({H^+})}}{{c(N{H_4}^+)}}$增大 | |
| D. | C(s)+H2O(g)?CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
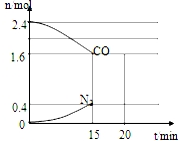 CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:
CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
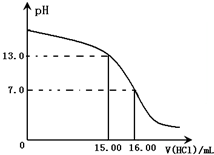 Ⅰ.某研究性学习小组用一定物质的量浓度的盐酸滴定10.00mL某浓度的NaOH溶液,滴定时使用pH计精确测量滴定过程中溶液的pH变化(温度为25℃),并绘制出滴定过程中溶液pH的变化曲线(如图).
Ⅰ.某研究性学习小组用一定物质的量浓度的盐酸滴定10.00mL某浓度的NaOH溶液,滴定时使用pH计精确测量滴定过程中溶液的pH变化(温度为25℃),并绘制出滴定过程中溶液pH的变化曲线(如图).| 实验步骤 | 设计这一步骤的目的 |
| (1)将配制的氢氧化钠溶液加热 | ① |
| (2)在加热后的溶液中滴加酚酞,并在上方滴一些植物油 | ②利用植物油隔绝空气 |
| 实验方法 | 观察到的现象 | 结论 |
| 方案一:分别配制不同物质的量浓度的氢氧化钠溶液,然后各滴加数滴酚酞溶液. | 浓度大的溶液中红色会消失 | 红色消失与氢氧化钠溶液的浓度大小有关 |
| 方案二:向原红色消失的溶液中加 ①(填试剂名称) | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(g)△H=-48.4 kJ•mol-1 | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-5517.6 kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=+5517.6 kJ•mol-1 | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-48.4 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
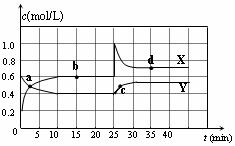
| A. | 图中的两条曲线,X表示NO2浓度随时间的变化曲线 | |
| B. | 前10 min内用v(N2O4)=0.02 mol/(L•min) | |
| C. | 25 min时,NO2转变为N2O4的反应速率增大,其原 因是将密闭容器的体积缩小为1L | |
| D. | 该温度下反应的平衡常数 K=1.11 L/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3溶液 | B. | 盐酸酸化的BaCl2溶液 | ||
| C. | KSCN溶液 | D. | HNO3酸化的Ba(NO3)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com