
| A£® | NH3 | B£® | N2 | C£® | CO2 | D£® | H2 |
·ÖĪö øł¾ŻŅŃÓŠµÄÖŖŹ¶½ųŠŠ·ÖĪö½ā“š£¬ÄÜÓėÅØĮņĖį·“Ó¦µÄĘųĢå²»ÄÜÓĆÅØĮņĖįøÉŌļ£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗA”¢°±ĘųÄÜÓėÅØĮņĖį·“Ó¦£¬²»æÉŅŌÓĆÅØĮņĖįøÉŌļ£¬¹ŹAŃ”£»
B”¢µŖĘų²»ÓėÅØĮņĖį·“Ó¦£¬æÉŅŌÓĆÅØĮņĖįøÉŌļ£¬¹ŹB²»Ń”£»
C”¢¶žŃõ»ÆĢ¼²»ÓėÅØĮņĖį·“Ó¦£¬æÉŅŌÓĆÅØĮņĖįøÉŌļ£¬¹ŹC²»Ń”£»
D”¢ĒāĘų²»ÓėÅØĮņĖį·“Ó¦£¬æÉŅŌÓĆÅØĮņĖįøÉŌļ£¬¹ŹD²»Ń”£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éÅØĮņĖįµÄŠŌÖŹ£¬ÕĘĪÕ³£¼ūµÄĪļÖŹµÄŠŌÖŹŅŌ¼°øÉŌļ¼ĮµÄŹ¹ÓĆ·¶Ī§ŹĒÕżČ·½ā“š±¾ĢāµÄ¹Ų¼ü£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
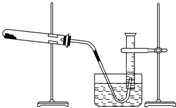 Ä³Ń§ÉśĄūÓĆĀČĖį¼Ų·Ö½āÖĘŃõĘųµÄ·“Ó¦£¬²ā¶ØŃõĘųµÄĦ¶ūÖŹĮ棬ŹµŃé²½ÖčČēĻĀ£ŗ
Ä³Ń§ÉśĄūÓĆĀČĖį¼Ų·Ö½āÖĘŃõĘųµÄ·“Ó¦£¬²ā¶ØŃõĘųµÄĦ¶ūÖŹĮ棬ŹµŃé²½ÖčČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
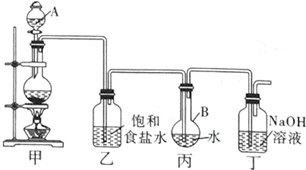
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓÉÖŹ×ÓŗĶµē×Ó¹¹³É | B£® | ÓÉŌ×ÓŗĖŗĶŗĖĶāµē×Ó¹¹³É | ||
| C£® | ÓÉÖŹ×ÓŗĶÖŠ×Ó¹¹³É | D£® | ÓÉÖŠ×ÓŗĶµē×Ó¹¹³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē½ā±„ŗĶBaCl2ČÜŅŗ”” Ņõ¼«£ŗBa2++2e-=Ba | |
| B£® | µē½āCu£ØNO3£©2ČÜŅŗ Ņõ¼«£ŗCu2++2e-=Cu | |
| C£® | µē½āČŪČŚNaClŅõ¼«£ŗNa++e-=Na | |
| D£® | µē½āNaOHČÜŅŗ Ńō¼«£ŗ4OH--4e-=2H2O+O2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
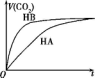 µČĢå»ż”¢ÅØ¶Č¾łĪŖ0.2mol•L-1µÄČżÖÖČÜŅŗ£ŗ¢ŁHAČÜŅŗ”¢¢ŚHBČÜŅŗ”¢¢ŪNaHCO3ČÜŅŗ£¬ŅŃÖŖ½«¢Ł¢Ś·Ö±šÓė¢Ū»ģŗĻ£¬ŹµŃé²āµĆĖł²śÉśµÄCO2ĘųĢåĢå»ż£ØV£©Ėꏱ¼ä£Øt£©±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
µČĢå»ż”¢ÅØ¶Č¾łĪŖ0.2mol•L-1µÄČżÖÖČÜŅŗ£ŗ¢ŁHAČÜŅŗ”¢¢ŚHBČÜŅŗ”¢¢ŪNaHCO3ČÜŅŗ£¬ŅŃÖŖ½«¢Ł¢Ś·Ö±šÓė¢Ū»ģŗĻ£¬ŹµŃé²āµĆĖł²śÉśµÄCO2ĘųĢåĢå»ż£ØV£©Ėꏱ¼ä£Øt£©±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ĖįŠŌ£ŗHB£¾HA£¾H2CO3 | |
| B£® | ·“Ó¦½įŹųŗóĖłµĆĮ½ČÜŅŗÖŠ£ŗc£ØA-£©£¾c£ØB-£© | |
| C£® | ÉĻŹöČżÖÖČÜŅŗÖŠÓÉĖ®µēĄėµÄc£ØOH-£©Ļą¶Ō“󊔣ŗNaHCO3£¾HA£¾HB | |
| D£® | HAČÜŅŗŗĶNaHCO3ČÜŅŗ·“Ó¦ĖłµĆµÄČÜŅŗÖŠ£ŗc£ØA-£©+c£ØHA£©=0.1 mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
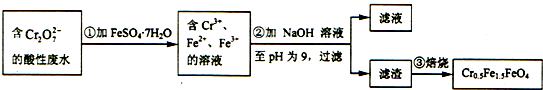
| A£® | øł¾ŻµŚ¢Ł²½·“Ó¦æÉÖŖ»¹ŌŠŌ£ŗCr3+“óÓŚFe2+ | |
| B£® | µŚ¢Ś²½¹żĀĖµĆµ½µÄĀĖŌüÖŠÖ÷ŅŖ³É·ÖĪŖCr£ØOH£©3”¢Fe£ØOH£©2£¬²»ŗ¬Fe£ØOH£©3 | |
| C£® | ÓūŹ¹1LøĆ·ĻĖ®ÖŠµÄCr2O72-ĶźČ«×Ŗ»ÆĪŖCr0.5Fe1.5FeO4£¬ĄķĀŪÉĻŠčŅŖ¼ÓČė27.8g FeSO4•7H2O | |
| D£® | µŚ¢Ū²½øßĪĀ±ŗÉÕ¹ż³ĢÓƵ½µÄÖ÷ŅŖŹµŃéŅĒĘ÷ÖŠŹōÓŚ¹čĖįŃĪÖŹµÄÓŠ£ŗ¾Ę¾«µĘ”¢Õō·¢Ćó”¢ÄąČż½Ē |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6Ģå»ż | B£® | 4Ģå»ż | C£® | 3Ģå»ż | D£® | ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com