
在强碱的无色溶液中,下列各组离子能大量共存的是( )
A. K+、Na+、NO3-、Br- B.Na+、NH4+、NO3-、Cl-
C.K+、Na+、HCO3- 、NO3- D.K+、Cu2+、Cl-、SO42-
科目:高中化学 来源:2016-2017学年浙江省杭州市五县七校高一上期中化学试卷(解析版) 题型:选择题
以下说法正确的是
A.1 mol O的质量为16 g B.1 mol氮的质量为 28 g/mol
C.1 mol C的质量为12 g/mol D.1 mol 氢的质量为1 g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省济宁市历城区高二上期中化学试卷(解析版) 题型:填空题
水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g) CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。
⑵上述反应达到平衡后,将体系 中的C(s)部分移走,平衡将 (填序号)。
中的C(s)部分移走,平衡将 (填序号)。
A.向左移 B.向右移 C.不移动
⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。
A.单位体积内每消耗1molCO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
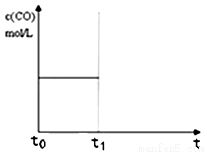
⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线:
①缩小容器体积(用实线表示)。
②降低温度(用虚线表示)。
⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g) CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省济宁市历城区高二上期中化学试卷(解析版) 题型:选择题
下列依据热化学方程式得出的结论正确的是 ( )
A.已知2SO2(g)+O2 2SO3(g)为放热反应,则SO2的能量一
2SO3(g)为放热反应,则SO2的能量一 定高于SO3的能量
定高于SO3的能量
B.已知C(石墨,s)=C(金刚石,s) △H﹥0,则金刚石比石墨稳定
C.已知H+(aq)+OH–(aq)=H2O(1) △H = -57.3kJ·mol-1,则任何酸碱中和的反应热均为57.3 kJ
D.已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2;则△H1﹤△H2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省天门市三校高一上学期期中化学试卷(解析版) 题型:推断题
某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是 .
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失.说明原溶液中肯定存在的离子 ,有关的离子方程式为 .
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明原溶液中肯定有 ,有关的离子方程式为 .
(4)原溶液可能大量存在的阴离子是下列的 .
A.Cl﹣ B.NO3﹣ C.CO32﹣ D.OH﹣.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省天门市三校高一上学期期中化学试卷(解析版) 题型:选择题
下列各项说法正确的是( )
①氢氧化铁胶体中,H+、K+、S2-、Br-能大量共存
②向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
③沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
④明矾可用作净水剂
⑤向饱和FeCl3溶液中滴加氢氧化钠溶液,可制取Fe(OH)3胶体
A.①③④ B.①②③④ C.②④ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省天门市三校高二上学期期中化学试卷(解析版) 题型:选择题
关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是 ( )
A.水电离出的c(H+):②>①
B.c(NH4+):③>①
C.①和②等体积混合后的溶液:c(H+) = c(OH- ) + c(NH3·H2O)
D.①和③等体积混合后显碱性,c(NH4+)>c(Cl-)>c(NH3·H2O )
查看答案和解析>>
科目:高中化学 来源:2017届广西钦州市高新区高三11月月考化学试卷(解析版) 题型:实验题
SO2随意排放会造成严重的大气污染。下列是某小组同学设计处理烟气(主要含SO2、N2、O2、粉尘)中SO2的方法。
(1)方法一:利用氯碱工业产品处理SO2的烟气,流程如下:
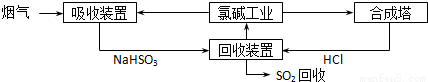
①“吸收装置”中发生反应的离子方程式_____________________。
②合成塔中每合成1mol气体放出热量92.3kJ(25℃、101kPa),反应的热化学方程式_____________。
③上述流程中循环利用的物质是____________________。
(2)方法二:利用FeCl3溶液氧化吸收烟气中SO2
①该反应的离子方程式________________________(反应a)。为验证该反应,同学们将SO2通入0.05mol/LFeCl3溶液中,溶液很快由 黄色变为红褐色;将溶液长时间放置后,最终变
黄色变为红褐色;将溶液长时间放置后,最终变 为浅绿色。关于红褐色液体,以下是同学们的分析推测
为浅绿色。关于红褐色液体,以下是同学们的分析推测 与
与 实验。
实验。
分析推测 | 实验步骤及现象 |
甲:生成了Fe(OH)3胶体 乙: Fe3++6SO2 | I、制备Fe(OH)3胶体并检验 II、分别向Fe(OH)3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
②利用胶体的_________________(填性质)可以检验步骤I中是否得到了Fe(OH)3胶体。
③根据反应b说明步骤II中液体颜色变化的原因是______________________(用离子方程式及必要的文字说明)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com