
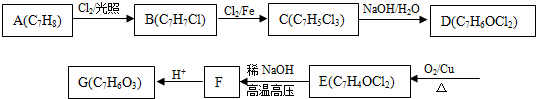
 ,A在光照条件下与氯气发生侧链上的取代生成B为
,A在光照条件下与氯气发生侧链上的取代生成B为 ,B在铁粉做催化剂的条件下发生苯环上的取代生成C为
,B在铁粉做催化剂的条件下发生苯环上的取代生成C为 ,C在碱性条件下水解发生取代反应得D为
,C在碱性条件下水解发生取代反应得D为 ,D被氧化得E为
,D被氧化得E为 ,E与稀氢氧化钠在高温高压的条件下生成F为
,E与稀氢氧化钠在高温高压的条件下生成F为 ,F酸化得G为
,F酸化得G为 ,据此答题.
,据此答题. ,A在光照条件下与氯气发生侧链上的取代生成B为
,A在光照条件下与氯气发生侧链上的取代生成B为 ,B在铁粉做催化剂的条件下发生苯环上的取代生成C为
,B在铁粉做催化剂的条件下发生苯环上的取代生成C为 ,C在碱性条件下水解发生取代反应得D为
,C在碱性条件下水解发生取代反应得D为 ,D被氧化得E为
,D被氧化得E为 ,E与稀氢氧化钠在高温高压的条件下生成F为
,E与稀氢氧化钠在高温高压的条件下生成F为 ,F酸化得G为
,F酸化得G为 ,
, ,G的结构简式为
,G的结构简式为 ,
, ;
; ;
;  ,E分子中含氧官能团的名称是醛基,故答案为:取代反应;醛基;
,E分子中含氧官能团的名称是醛基,故答案为:取代反应;醛基; 、
、 、
、 ,
, ;
; ;
; ;
; ,
, .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将高温水蒸气通过炽热的铁粉,铁粉变红色 |
| B、向Fe(OH)3胶体中滴加稀H2SO4,先出现沉淀,后沉淀溶解 |
| C、将市售食盐溶于水,滴加淀粉溶液不变蓝色,说明不是加碘盐 |
| D、Cu的金属活泼性比Fe弱,故水库铁闸门上接装铜块可减缓铁腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
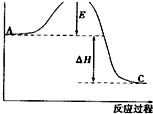 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.请回答下列问题:| 1 |
| 3 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
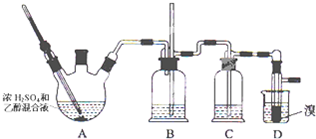
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g?cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
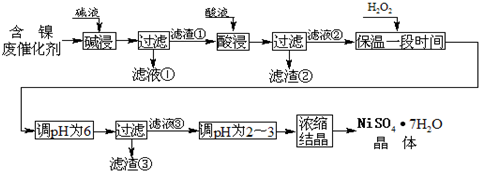
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

| A、沉淀1加酸部分溶解,则含Mg2+和SO42- |
| B、可能含Na+、Cl- |
| C、沉淀2加酸溶解,则含Al3+ |
| D、气体1遇水显碱性,则含NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com