
【题目】已知:[FeCl4(H2O)2]-为黄色,下列实验所得结论不正确的是
① | ② | ③ | ④ |
0.1mol/L Fe2(SO4)3溶液 |
酸化的0.1mol/L Fe2(SO4)3溶液 |
酸化的0.1mol/L Fe2(SO4)3溶液 |
0.1mol/L FeCl3溶液 |
加热前溶液为浅黄色,加热后颜色变深 | 加热前溶液接近无色,加热后溶液颜色无明显变化 | 加入NaCl后,溶液立即变为黄色,加热后溶液颜色变深 | 加热前溶液为黄色,加热后溶液颜色变深 |
注:加热为微热,忽略体积变化。
A. 实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3
B. 实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C. 实验③中,存在可逆反应: Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-
[FeCl4(H2O)2]-
D. 实验④,可证明升高温度,Fe3+水解平衡正向移动
【答案】D
【解析】
A. 实验①中,0.1mol/LFe2(SO4)3溶液加热前溶液为浅黄色,加热后颜色变深,说明升高温度水解程度增大,颜色加深,故Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3,选项A正确;
B. 实验②中,酸化的0.1mol/LFe2(SO4)3溶液加热前溶液接近无色,加热后溶液颜色无明显变化,说明温度升高几乎不能引起变化,则酸化对Fe3+水解的影响程度大于温度的影响,选项B正确;
C. 实验③中,酸化的0.1mol/LFe2(SO4)3溶液加入NaCl后,溶液立即变为黄色,则氯离子影响平衡移动,加热后溶液颜色变深,则存在可逆反应: Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-,选项C正确;
[FeCl4(H2O)2]-,选项C正确;
D. 实验④,加热前溶液为黄色,加热后溶液颜色变深,水解平衡或平衡Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-均可能使颜色变深,故不可证明升高温度,Fe3+水解平衡正向移动,选项D不正确。
[FeCl4(H2O)2]-均可能使颜色变深,故不可证明升高温度,Fe3+水解平衡正向移动,选项D不正确。
答案选D。


科目:高中化学 来源: 题型:
【题目】LiNiO2是一种前景很好的锂离子电池正极材料。当温度高于850°C时,LiNiO2会分解。请按要求回答下列问题:
(1)LiNiO2中Ni的化合价为___________,工业上用Ni(OH)2与LiOH的混合物在空气流中加热到700~800°C制得 LiNiO2,该反应的化学方程式为___________,加热温度不宜过高的原因是_________,工业上也可用LiNO3代替上述工艺中的LiOH,存在的缺点可能是_______。
(2)以废旧二次电池为原料回收利用合成Ni(OH)2的工艺如下:

已知:酸浸后滤液中含有Ni2+、Al3+、Fe3+、Mn2+;
Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,Ksp[Ni(OH)2]=1.6×10-14;
①滤渣Ⅱ为___________。
②“氧化除锰”是将锰元素最终转化为MnO2而除去,反应历程如下:
i.5S2O82-+2Mn2++8H2O=2MnO4-+10SO42-+16H+;
ii.______________________(用离子方程式表示)。
③转化操作后,还需经过过滤、洗涤、烘干得到产品。检验Ni(OH)2是否洗涤干净的实验操作是___________。
④调pH=5操作时,已知溶液中Ni2+浓度为2.0mol/L,则“滤渣II”中是否存在Ni(OH)2沉淀?___________(列式计算,并使用必要的文字说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿与铜蓝矿都是天然含硫铜矿,在地壳中二者常伴生存在。现取一份该伴生矿样品,经检测后确定仅含Cu2S、CuS和惰性杂质。为进一步确定其中Cu2S、CuS的含量,某同学进行了如下实验:
①取2.6g样品,加入200.0mL0.2000mol·L-1酸性KMnO4溶液,加热(硫元素全部转化为SO42-),滤去不溶杂质;
②收集滤液至250mL容量瓶中,定容;
③取25.00mL溶液,用0.1000mol·L-1FeSO4溶液滴定,消耗20.00mL;
④加入适量NH4HF2溶液(掩蔽Fe3+和Mn2+,使其不再参与其他反应),再加入过量KI固体,轻摇使之溶解并发生反应:2Cu2++4I-=2CuI+I2;
⑤加入2滴淀粉溶液,用0.1000mo1·L-1Na2S2O3溶液滴定,消耗30.00mL(已知:2S2O32-+I2=S4O62-+2I-)。
回答下列问题:
(1)写出Cu2S溶于酸性KMnO4溶液的离子方程式:___________;
(2)配制0.1000mol· L-1FeSO4溶液时要用煮沸过的稀硫酸,原因是___________,配制过程中所需玻璃仪器除了烧杯、玻璃棒、容量瓶外还有___________;
(3)③中取25.00mL待测溶液所用的仪器是___________;
(4)⑤中滴定至终点时的现象为___________;
(5)混合样品中Cu2S和CuS的含量分别为_________%、_________%(结果均保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据能量变化示意图,下列说法正确的是
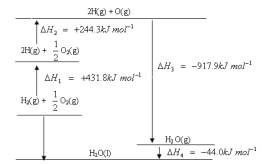
A. H2在O2中燃烧生成气态水的过程中吸收能量
B. 断开1mol H2O(g)所含的共价键共放出917.9kJ的能量
C. H2O(g)比H2O(l)更稳定
D. H2在O2中燃烧生成液态水的热化学方程式为:2H2(g) + O2(g) == 2H2O(l) ![]() H = -571.6 kJ·mol-1
H = -571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:X(g)+2Y(g)![]() 3Z(g) △H=-akJ·mol-1(a>0)。下列说法正确的是
3Z(g) △H=-akJ·mol-1(a>0)。下列说法正确的是
A. 达到平衡状态时,放出的热量一定小于a kJ
B. 向体系中加入X(g)时,正、逆反应速率一定都增大
C. 当容器内的压强保持不变时,则反应一定达到平衡状态
D. 若Y与Z的物质的量之比保持不变,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填写:
(1)二氧化碳的电子式:______________;小苏打的化学式:________________;质子数为6、中子数为6的原子结构示意图____________________。
(2)氯气与氢氧化钠溶液反应的化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证某单质与某浓酸在加热条件下反应生成气体甲和乙的成分,某同学设计了如下实验装置图,其中A装置用于检验气体甲:

(1)写出该非单质与浓酸反应的化学方程式:___________________________________。
(2)证明气体中含有乙的实验现象是___________________________________________。
(3)为除去甲,收集纯净干燥的气体乙,某同学欲选用下列装置:

则按气流从左到右,各接口连接顺序正确的是______________。
A.dcabh B.feabh C.feabg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中,反应A+2B![]() C分别在三种不同实验条件下进行,它们的起始状态均为c(A) = 0.100 mol·L-1 c(B) = 0.200 mol·L-1 、c(C) = 0 mol·L-1 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
C分别在三种不同实验条件下进行,它们的起始状态均为c(A) = 0.100 mol·L-1 c(B) = 0.200 mol·L-1 、c(C) = 0 mol·L-1 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是

A. 反应的平衡常数:①<② B. 反应A+2B![]() C的△H >0
C的△H >0
C. 实验②平衡时B的转化率为60% D. 实验③平衡时c(C) = 0.04 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com