
现有甲、乙、丙三种晶胞,如图所示。
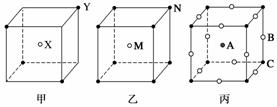
甲中X处于晶胞中心;乙中M处于晶胞中心;丙中A处于晶胞中心,B处于棱上,C处于顶点。由此可知:
(1)甲晶胞中X与Y的个数之比为________________________________________。
(2)乙晶胞中M与N的个数之比为________________________________________。
(3)丙的化学式是_______________________________________________________。
科目:高中化学 来源: 题型:
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两个成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满。
请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为______________________。
(2)B的氯化物的熔点比D的氯化物的熔点________(填“高”或“低”),理由是
________________________________________________________________________
________________________________________________________________________。
(3)F的核外电子排布式是______________________________,F的高价离子与A的简单氢化物形成的配离子的化学式为__________。
(4)A、F形成某种化合物的晶胞结构如下图所示(其中A显-3价),则其化学式为
____________。(每个球均表示1个原子)
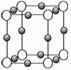
(5)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,则其化学式为____________________,其晶体中所含的化学键类型为________________,其晶体类型是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知C3N4晶体很可能具有比金刚石更大的硬度,且原子间均以单键结合。下列关于C3N4晶体的说法正确的是( )
A.C3N4是分子晶体
B.C3N4晶体中,C—N键的键长比金刚石中的C—C键的键长要长
C.C3N4晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子
D.C3N4晶体中微粒间通过分子间作用力结合
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.含有非极性共价键的化合物分子一定是非极性分子
B.原子晶体中只存在非极性共价键
C.冰主要是水分子通过氢键作用而形成的分子晶体
D.若元素R的含氧酸的酸性大于元素Q的含氧酸的酸性,则非金属性R大于Q
查看答案和解析>>
科目:高中化学 来源: 题型:
三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型的叙述,不正确的是( )
A.PCl3分子中P采用sp3杂化
B.PCl3分子中P—Cl键属于极性共价键
C.PCl3分子中三个共价键键能、键角均相等
D.PCl3是非极性分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com