
 .
.
分析 (1)最外层有5个电子,由同主族位置和元素周期律可知,非金属性N>As;
(2)As2O5分解为As2O3需要吸收的热量为-619kJ/mol-(-914.6kJ/mol)=+295.4 kJ•mol-1,以此书写热化学方程式;
(3)①发生AsO43-+2I-+2H+?AsO33-+I2+H2O,C1棒为负极,发生2I--2e-=I2,C2为正极发生还原反应;
②向B中滴加过量浓NaOH溶液,发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极.
(4)①根据As2O5与NaOH溶液反应生成盐和水书写离子方程式;
②上述混合液用0.02500mol•L-1的I2溶液滴定,消耗I2溶液20.00mL,根据AsO33-+I2+H2O═AsO43-+2I-+2H+反应,则消耗AsO33-的物质的量为0.02500mol•L-1×20.00×10-3L=5×10-4mol,新生成的AsO43-的物质的量也为5×10-4mol;设原As2O5 的物质的量:x,
由As2O5→2AsO43-,则由As2O5 与氢氧化钠反应生成的AsO43-的物质的量为2x,后又加入过量的KI,又发生AsO42-+2I-+2H+═AsO32-+I2+H2O,
析出的I2又用0.1000mol•L-1的Na2S2O3溶液滴定,发生反应为I2+2Na2S2O3=2NaI+Na2S4O6,消耗Na2S2O3溶液30.00mL,
所以有AsO43-~I2~2Na2S2O3,据消耗的Na2S2O3计算.
解答 解:(1)最外层有5个电子,则As位于第ⅤA族,由同主族位置和元素周期律可知,非金属性N>As,则As的气态氢化物的稳定性比NH3弱,
故答案为:ⅤA;弱;
(2)由图象可知,As2O5分解为As2O3需要吸收的热量为-619kJ/mol-(-914.6kJ/mol)=+295.4 kJ•mol-1,则热化学方程式As2O5(s)=As2O3(s)+O2(g)△H=+295.4 kJ•mol-1,
故答案为:As2O5(s)=As2O3(s)+O2(g)△H=+295.4 kJ•mol-1;
(3)①B中滴加浓盐酸时发生AsO43-+2I-+2H+?AsO33-+I2+H2O,A中C1棒为负极,发生2I--2e-=I2,C2为正极发生还原反应,电极反应为AsO42-+2H++2e-=AsO32-+H2O,
故答案为:AsO42-+2H++2e-=AsO32-+H2O;
②向B中滴加过量浓NaOH溶液,发生AsO33-+I2+2OH-?AsO43-+2I-+H2O,C2棒为负极,电子由负极流向正极,可观察到电流计指针向左偏,
故答案为:向左偏;
(4)①因为As2O5为碱性氧化物,与NaOH溶液反应生成盐和水,所以离子方程式为:As2O5+6OH-═2AsO43-+3H2O,故答案为:As2O5+6OH-═2AsO43-+3H2O;
②上述混合液用0.02500mol•L-1的I2溶液滴定,消耗I2溶液20.00mL,根据AsO33-+I2+H2O═AsO43-+2I-+2H+反应,
则消耗AsO33-的物质的量为0.02500mol•L-1×20.00×10-3L=5×10-4mol,新生成的AsO43-的物质的量也为5×10-4mol;
设原As2O5 的物质的量为x,
由As2O5→2AsO43-,则由As2O5 与氢氧化钠反应生成的AsO43-的物质的量为2x,
后又加入过量的KI,又发生AsO42-+2I-+2H+═AsO32-+I2+H2O,析出的I2又用0.1000mol•L-1的Na2S2O3溶液滴定,发生反应为I2+2Na2S2O3=2NaI+Na2S4O6,
消耗Na2S2O3溶液30.00mL,
所以有AsO43-~I2~2Na2S2O3
1 2
2x+5×10-4 0.1×30×10-3
解得:x=0.0005 mol
m(As2O5)=0.0005×230=0.115 g
故答案为:0.115.
点评 本题考查较综合,涉及元素的位置及元素周期律、热化学方程式、原电池的工作原理等,注重高考高频考点的考查,侧重学生分析能力及知识迁移应用能力的考查,(4)为解答的难点,注意利用反应方程式中各物质之间的关系计算,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解后,c(Na2SO4)不变,且溶液中有晶体析出 | |
| B. | 电解池的阳极反应式为:4OH--4e-═2H2O+O2↑ | |
| C. | 蓄电池放电时,每消耗0.1molPb,共生成0.1molPbSO4 | |
| D. | 蓄电池中每生成2molH2O,电解池中就消耗1molH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | R | W | X | Y | Z |
| 化合价 | -4 | +1 | -4 | -2 | -1 |
| A. | 离子还原性:Y2-<Z- | B. | 离子半径W+>Z- | ||
| C. | 气态氢化物稳定性:RH4<XH4 | D. | 酸性:H2YO4<HZO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol H2O的质量为18g | |
| B. | 摩尔是表示物质微粒数目的一个物理量 | |
| C. | 3.01×1023个SO2分子的质量为64g | |
| D. | 标准状况下,1 mol任何物质体积均约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.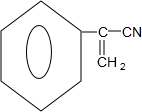 ,E中含氧官能团的名称为羧基.
,E中含氧官能团的名称为羧基. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ | |
| B. | 向NH4HSO4溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全Ba2++H++OH-+SO42-=BaSO4↓+H2O | |
| C. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO3- | |
| D. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液2Fe2++2H++H2O2=2Fe3++2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com