
| A. | △H4=△H3+△H2+△H1 | B. | △H4=△H3+2△H2+2△H1 | ||
| C. | △H4=△H3+2△H2-2△H1 | D. | △H4=△H3+2△H2-△H1 |
分析 由CO(g)+2H2(g)═CH3OH(g)△H1①;
2H2(g)+O2(g)═2H2O(l)△H2 ②;
2CO(g)+O2(g)═2CO2(g)△H3③;
结合盖斯定律可知,③+②×2-①×2得到2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l),以此来解答.
解答 解:由CO(g)+2H2(g)═CH3OH(g)△H1①;
2H2(g)+O2(g)═2H2O(l)△H2 ②;
2CO(g)+O2(g)═2CO2(g)△H3③;
结合盖斯定律可知,③+②×2-①×2得到2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l),
则△H4=△H3+2△H2-2△H1,
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应的关系、焓变的关系为解答的关键,侧重分析与应用能力的考查,注意盖斯定律的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 红热的铜丝在硫蒸汽中燃烧,产生黑色固体 | |
| B. | 碘水中加入少量CCl4,振荡静置后,下层颜色变浅,上层颜色变为紫色 | |
| C. | 往溴水中加入碘化钠溶液,溴水变为无色 | |
| D. | 氢气在Cl2中燃烧产生白色的烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
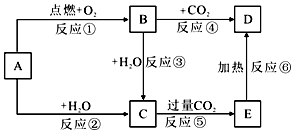
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
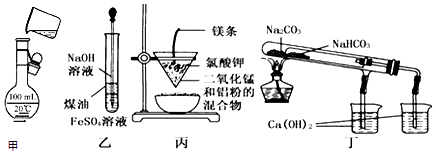
| A. | 用甲图所示装置将溶液定容到100 mL | |
| B. | 用乙图装置制备Fe(OH)2 | |
| C. | 用丙图装置可制得金属锰 | |
| D. | 用丁图装置验证NaHCO3和Na2CO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
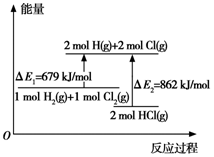
| A. | △E1是该反应的活化能 | B. | △E2是2 mol H-Cl键的总键能 | ||
| C. | 加入催化剂可以改变反应的焓变 | D. | 该反应是一个放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
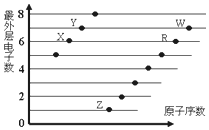
| A. | X与W形成的化合物中只有共价键 | B. | X与Z形成的化合物中只有离子键 | ||
| C. | 元素的非金属性:X>R>W | D. | 简单离子的半径:W>R>X |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
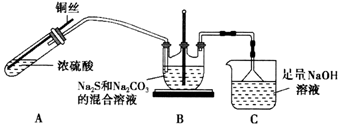
| 序号 | 操作及现象 | 结论 |
| ① | 取少量Al(OH)3粉末于试管中,滴加适量溶液,振荡,白色粉末溶解 | 溶质中一定含有NaOH |
| ② | 取2nL溶液于试管中,滴加足量氯水,氯水褪色丙有气泡产生,再滴加几滴Ba(NO3)2溶液,有白色沉淀产生 | 溶质为NaOH和 Na2CO3、Na2SO3 |
| 取2mL溶液于试管中,若 先加入足量稀硝酸,产生气泡,再滴入几滴Ba(NO3)2溶液,无沉淀产生 | 溶质为为NaOH和Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com