
【题目】科学家研究发现普通盐水在无线电波的照射下可以燃烧,其原理是无线电频率可以削弱盐水中所含元素原子之间的“结合力”,释放出氢原子和氧原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述中“结合力”的实质是
A. 离子键B. 共价键C. 范德华力D. 氢键
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室制备1,2﹣二溴乙烷的反应原理如下:CH3CH2OH ![]() CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如右图所示,有关数据如表:
CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如右图所示,有关数据如表: 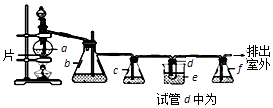
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
回答下列问题:
(1)在装置c中应加入(选填序号),其目的是吸收反应中可能生成的酸性气体. ①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的 层.(填“上”或“下”)
(3)判断d管中制备二溴乙烷反应已结束的最简单方法是 .
(4)若产物中有少量未反应的Br2 , 最好用(填正确选项前的序号)洗涤除去. ①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)以1,2﹣二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2﹣二溴乙烷通过(①)反应制得(②),②通过(③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯. ①(填反应类型),其化学方程式 .
②(填反应类型).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1是某研究性学习小组设计制取氯气并以氯气为原料进行特定反应的装置.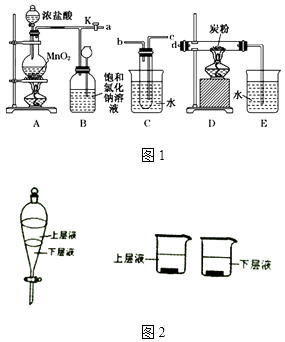
(1)要将C装置接入B和D之间,正确的接法是:a→→→d;
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯,Cl2通过C装置后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为 .
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 , B的作用是 .
(4)用量筒量取20mL E中溶液,倒入已检查完气密性良好的分液漏斗中,然后再注入10mL CCl4 , 盖好玻璃塞,振荡,静置于铁架台上(如图2),等分层后取上层液和下层液,能使有色布条褪色的是(填“上层液”或“下层液”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】举世瞩目的中国探月工程三期再入返回试验器于2014年10月24日凌晨成功发射,为实现月球采样和首次地月往返踏出了成功的第一步.探月工程三期的主要目标是实现无人自动采样返回,突破月面采样、月面上升、月球轨道交会对接等核心关键技术.已知所用火箭推进剂为肼 (N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料. 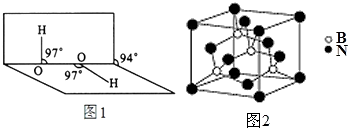
请回答下列问题:
(1)N2H4、H2O2分子中电负性最大的元素在周期表中的位置为 , 第一电离能最大的元素为 .
(2)钛的原子序数为22,其基态电子排布式示意图为 .
(3)1mol N2H4分子中含有的键数目为 .
(4)H2O2分子结构如图1,其中心原子杂化轨道为 , 估计它难溶于CS2 , 简要说明原因
(5)氮化硼其晶胞如图2所示,则处于晶胞顶点上的原子的配位数为 , 若立方氮化硼的密度为ρ gcm﹣3 , 阿伏加德罗常数为NA , 则两个最近N原子间的距离为cm.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重要有机物M和N常用于交联剂、涂料、杀虫剂等,合成路线如图所示: 
已知:
i ![]()
ii 
iii N的结构简式: ![]()
请回答下列问题:
(1)A中含氧官能团的名称为 , 由A生成B的反应类型为 .
(2)Z的名称为
(3)1molM在一定条件下发生加成反应,最多消耗molH2 .
(4)由B生成C的反应①的化学方程式为 .
(5)由Y生成D的化学方程式为 .
(6)G的同分异构体有多种,其中与G具有相同官能团的同分异构体有种,写出核磁共振氢谱有5组峰值,且峰值比为2:2:2:1:1的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡常用于染色的媒染剂等,工业上常用氯气与金属锡反应制备四氯化锡.已知SnCl4为无色液体,熔点﹣33℃,沸点114℃,极易水解,在潮湿的空气中发烟.实验室可用如图装置合成四氯化锡(夹持装置略). 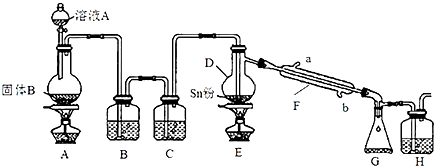
(1)装置D的名称为;
(2)冷凝水应从(填“a”或“b”)口进入F中;
(3)装置A中固体B为黑色粉末,写出烧瓶中发生反应的化学反应方程式为;
(4)假设没有装置C,在D中除生成SnCl4外,可能得到的副产物为;
(5)装置E中加热的目的是、;
(6)装置H中盛放足量的FeBr2溶液可吸收尾气中的氯气,其反应的离子反应方程式为 .
(7)该实验装置存在设计缺陷,你的改进措施为 .
(8)若装置A中标准状况下生成6.72L气体,假设不计气体损耗且Sn足量,反应完毕后在G 中锥形瓶里收集到37.20g SnCl4 , 则SnCl4的产率为 . (已知SnCl4相对分子质量为261)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2010年4月中旬全球核安全峰会在华盛顿举行,发展核电、制裁核武器发展是会议主题。各式各样电池的发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
A. 手机上用的锂电池属于二次电池
B. 锌锰干电池中,锌电极是正极
C. 氢氧燃料电池工作时氢气在负极被还原
D. 太阳能电池的主要材料为二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A. ①和② B. ①和④ C. ③和④ D. ①和③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.同温同压下甲烷和氧气的密度之比为2:1
B.1 g甲烷和1 g氧气的原子数之比为5:1
C.等物质的量的甲烷和氧气的质量之比为2:1
D.在标准状况下等质量的甲烷和氧气的体积之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com