

分析 碱式碳酸铜受热易分解,生成黑色的氧化铜.甲酸铜的溶解度随温度的升高而变大,需趁热过滤.根据“相似相溶原理”可知甲酸铜易溶于水,难溶于有机溶剂,
Ⅰ.①将一定量CuSO4•5H2O晶体和NaHCO3固体一起放到研钵中研磨会增大接触面积,加快反应速率;
②碱式碳酸铜受热易分解,生成黑色的氧化铜;
Ⅱ.a.甲酸铜的溶解度随温度的升高而变大;
b.根据“相似相溶原理”可知甲酸铜易溶于水,难溶于有机溶剂;
解答 解:碱式碳酸铜受热易分解,生成黑色的氧化铜.甲酸铜的溶解度随温度的升高而变大,需趁热过滤.根据“相似相溶原理”可知甲酸铜易溶于水,难溶于有机溶剂,
Ⅰ.①研磨的作用是把药品研细并混合均匀,
故答案为:研细并混合均匀;
②温度过高,Cu(OH)2•CuCO3会分解生成黑色的氧化铜,所以有黑色固体生成时说明温度过高,
故答案为:有黑色固体生成;
Ⅱ.a.甲酸铜的溶解度随温度的升高而变大,如果冷却,会有晶体析出,降低产率,因此需趁热过滤,
故答案为:防止甲酸铜晶体析出;
b.甲酸铜易溶于水,不能用蒸馏水洗涤,故需用乙醇进行洗涤,洗去晶体表面的液体杂质,
故答案为:洗去晶体表面的水和其它杂质.
点评 本题考查了制备方案的设计,题目难度不大,明确制备原理为解答关键,注意熟练掌握常见化学实验基本操作方法,试题侧重基础知识的考查,培养了学生的分析能力及化学实验能力.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:选择题
| A. | 同系物之间在化学性质上相似 | |
| B. | 同系物之间的物理性质随分子里碳原子数的递增,呈规律性的变化 | |
| C. | 同系物不可能是同分异构体 | |
| D. | 分子组成相差一个或几个CH2原子团的物质互称为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\stackrel{235}{92}$U和$\stackrel{238}{92}$U是中子数不同质子数相同的同种核素 | |
| B. | 质子数为53,中子数为78的碘原子:$\stackrel{131}{53}$I | |
| C. | 同种元素的原子均有相同的质子数和中子数 | |
| D. | 通过化学变化可以实现16O与18O间的相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
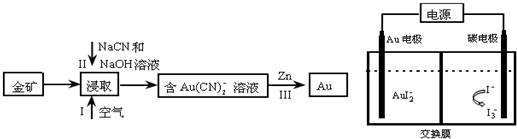
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
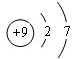 ,D离子的结构示意图:
,D离子的结构示意图: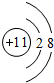 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
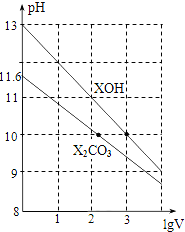
| A. | XOH是弱碱 | |
| B. | pH=10的两种溶液中的c(X+):XOH大于X2CO3 | |
| C. | 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2 | |
| D. | 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 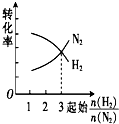 | B. | 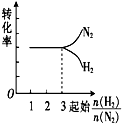 | C. | 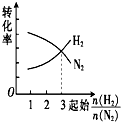 | D. | 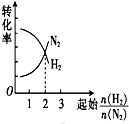 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com