
| A、Si |
| B、SiC |
| C、SiO2 |
| D、Na2SiO3 |
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| A、11.2 L H2和0.5 molCO2 |
| B、18 mL H2O(4℃)和2ⅹ105Pa,27℃32 g O2 |
| C、1 molCO和88 g CO2 |
| D、25℃,22.4 LCl2和含4 mol氧原子的H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
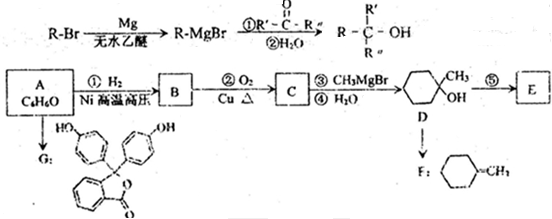
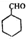 的合成路线流程图(无机试剂任选),方框内写有机物结构简式,在“→”上或下方写反应所需条件或试剂.
的合成路线流程图(无机试剂任选),方框内写有机物结构简式,在“→”上或下方写反应所需条件或试剂.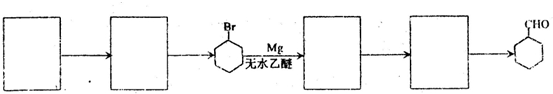
查看答案和解析>>
科目:高中化学 来源: 题型:
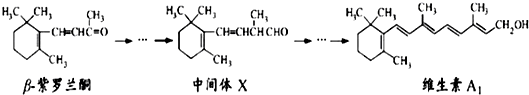
| A、β-紫罗兰酮可使酸性KMnO4溶液褪色 |
| B、1mol中间体X最多能与2molH2发生加成反应 |
| C、维生素A1不能氧化成醛 |
| D、维生素A1属于芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液滴入NaOH溶液中 |
| B、Ba(OH)2溶液滴入Al2(SO4)3溶液中 |
| C、盐酸滴入NaAlO2溶液中 |
| D、氨水滴入AlCl3溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ |
| B、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
| D、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
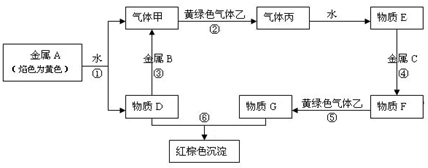
查看答案和解析>>
科目:高中化学 来源: 题型:
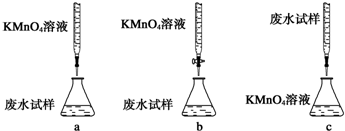
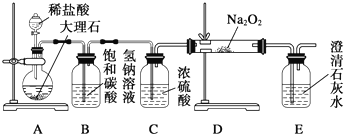
查看答案和解析>>
科目:高中化学 来源: 题型:
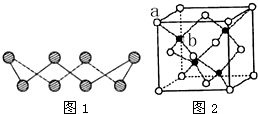 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com