
【题目】(1)原子序数大于4的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,据此推断:
①A和B所属周期数之差为___________
②A和B的核电荷数之差为____________(用含m、n的代数式表示)
③B和A的族序数之差为______________(用含m、n的代数式表示)
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。回答下列问题:
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为_____________;当B在A的下一周期时,B的原子序数为______________;
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________当B在A的下一周期时,B的原子序数为______________。
(3)某粒子的结构示意图为: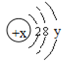 试回答:
试回答:
①当x-y=10时,该粒子为________(填“原子”或“阳离子”“阴离子”)
②当y=8时,该粒子可能是(写名称):_______、________、_______、_______、_______。
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式________________。
【答案】1 m+n 8-n-m x-n x+m x-m x+n 原子 氩原子 氯离子 硫离子 钾离子 钙离子) Al(OH)3+3H+=Al3++3H2O
【解析】
(1)①因Am+和Bn-核外电子排布相同,故A原子比B原子多一个电子层,故二者的周期数之差为1,故答案为:1;
②电子排布相同,则电子数相同,即ZA-m=ZB+n,则ZA-ZB=m+n,故答案为:m+n;
③B的负价为-n,则最高正价为8-n,即B的族序数为8-n,而A的族序数为m,B和A的族序数之差为8-n-m,故答案为:8-n-m;
(2)①A、B同在ⅠA族,当B在A的上一周期时,B和A的原子序数之差恰好为B所在周期的元素种类数,则B的原子序数为x-n;当B在A的下一周期时,A和B的原子序数之差恰好为A所在周期的元素种类数,则B的原子序数为x+m,故答案为:x-n;x+m;
②A、B同在ⅦA族时,A、B原子序数之差恰好为相邻两周期下一周期的元素种类数,与A、B同在ⅠA族相反,如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为x-m,当B在A的下一周期时,B的原子序数为 x+n,故答案为:x-m;x+n;
(3)①当x-y=10时,核内质子数为x,核外电子数为2+8+y,两者相等,所以该粒子为原子,故答案为:原子;
②当y=8时,该微粒的核外电子数为18,而离子中核内质子数不等于核外电子数,则该粒子的核内质子数为:20、19、18、17、16等,所以这些粒子为氩原子、氯离子、硫离子、钾离子、钙离子,故答案为:氩原子;氯离子;硫离子;钾离子;钙离子;
③y=3与y=7的元素最高价氧化物对应水化物分别为Al(OH)3和HClO4,反应离子方程式为Al(OH)3+3H+=Al3++3H2O,故答案为:Al(OH)3+3H+=Al3++3H2O。


科目:高中化学 来源: 题型:
【题目】如图所示表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。
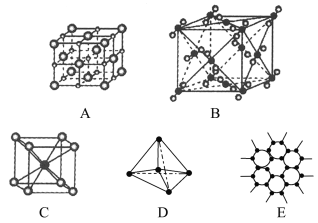
(1)其中代表金刚石的是(填编号字母,下同)________,其中每个碳原子与________个碳原子最接近且距离相等。金刚石属于________晶体。
(2)其中代表石墨的是________,其中每个正六边形占有碳原子数平均为________个。
(3)其中代表NaCl晶体的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(4)代表CsCl晶体的是________,它属于________晶体,每个Cs+与________个Cl-紧邻。
(5)代表干冰的是________,它属于________晶体,每个CO2分子与________个CO2分子紧邻。
(6)上述五种物质熔点由高到低的排列顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)下列关于金属及金属键的说法不正确的是______。(填字母代号)
a.金属键没有方向性与饱和性
b.金属键是金属原子与自由电子间的相互作用
c.金属熔沸点不同的原因可以用金属键强弱解释
d.电子气理论可解释金属材料的延展性,不能解释金属有良好的导电性
(2)钒广泛用于催化及钢铁工业,基态钒原子的价层电子排布图为_________________。
(3)二茂铁又叫双环戊二烯基铁[Fe(C5H5)2],熔点是172.5~173 ℃,100 ℃以上升华,二茂铁属于_____晶体。已知分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() )。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
)。已知二茂铁的每个茂环带有一个单位负电荷,则每个环中的大π键应表示为________________。
(4)铜可以形成一种离子化合物[Cu(NH3)4(H2O)2]SO4,若要确定[Cu(NH3)4(H2O)2]SO4是晶体还是非晶体,最科学的方法是对其进行______实验,其中阴离子的空间构型是_____,该化合物加热时首先失去的组分是H2O,原因是_______________________。
(5)最近发现,只含镁、镍和碳三种元素的晶体也具有超导性,该物质形成的晶体的立方晶胞结构如图所示。
①与Mg紧邻的Ni有________个。
②原子坐标参数可表示晶胞内部各原子的相对位置。该晶胞中原子的坐标参数为a为(0,0,0);b为(1/2,1/2,0);d为(1,1,1)。则c原子的坐标参数为_______。
③若晶胞中Ni、Mg之间的最短距离为a pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=______g·cm-3(用含a、NA的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A是分子式为![]() 的五元环状化合物,核磁共振氢谱有四组峰,且其峰面积之比为
的五元环状化合物,核磁共振氢谱有四组峰,且其峰面积之比为![]() ,有如图所示的转化:
,有如图所示的转化:

已知:
![]() 含羰基的化合物均能与格氏试剂发生如下反应:
含羰基的化合物均能与格氏试剂发生如下反应:![]()
![]()
![]()
![]() 两个羟基连在同一碳原子上极不稳定,易脱水:
两个羟基连在同一碳原子上极不稳定,易脱水: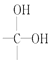 →
→![]() +H2O
+H2O
根据以上信息,回答下列问题:
![]() 写出化合物D中官能团的名称________。
写出化合物D中官能团的名称________。
![]() 写出化合物B、F的结构简式________、________。
写出化合物B、F的结构简式________、________。
![]() 的反应类型是________。
的反应类型是________。
![]() 写出D与
写出D与![]() 反应的化学方程式________________
反应的化学方程式________________![]() 写出
写出![]() 的化学方程式_______________________。
的化学方程式_______________________。
![]() 的属于芳香族化合物的同分异构体有________种,写出符合下列条件的A的一种同分异构体W的结构简式________。
的属于芳香族化合物的同分异构体有________种,写出符合下列条件的A的一种同分异构体W的结构简式________。![]() 不考虑立体异构
不考虑立体异构![]()
![]() 含有两个取代基
含有两个取代基 ![]() 苯环上的一氯代物只有两种
苯环上的一氯代物只有两种 ![]() 能与足量金属钠反应生成
能与足量金属钠反应生成![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】屈昔多巴( )可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等。以下是屈昔多巴的一种合成路线(通常
)可治疗直立性低血压所致头昏、头晕和乏力,帕金森病患者的步态僵直等。以下是屈昔多巴的一种合成路线(通常![]() 简写为BnCl,
简写为BnCl,![]() 简写为CbzCl ):
简写为CbzCl ):

回答下列问题:
(1)反应①的反应类型为_____________,其作用为_________________。
(2)屈昔多巴中所含的非含氧官能团名称为_______________,屈昔多巴分子中有___________个手性碳原子。
(3)反应②为加成反应,有机物X的名称为______________________。
(4)![]() 显________________性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:_______________________。
显________________性(填“酸”、“中”或“碱”),写出其与盐酸反应的化学方程式:_______________________。
(5)![]() 的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_______种,其中核磁共振氢谱为四组峰的结构简式为______________(任写一种)。
的同分异构体中,能与NaHCO3溶液反应生成CO2的二取代芳香化合物有_______种,其中核磁共振氢谱为四组峰的结构简式为______________(任写一种)。
(6)参照上述合成路线,以对羟基苯甲醛为原料(无机试剂任选),设计制备对羟基苯甲酸的合成路线:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质是大气污染物监测物之一;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为 。
(2)MX3-的空间构型 (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是 。
(4)根据等电子原理,WX分子的结构式为 。
(5)1 mol WX2中含有的σ键数目为 。
(6)H2X分子中X原子轨道的杂化类型为 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1923年,在汉阳兵工厂工作的我国化学家吴蕴初先生研制出了廉价生产味精的方案,并于1926年向英、美、法等化学工业发达国家申请专利。这也是历史上中国的化学产品第一次在国外申请专利。以下是利用该方法合成味精的流程![]() 部分产物及反应条件已省略
部分产物及反应条件已省略![]() :
:
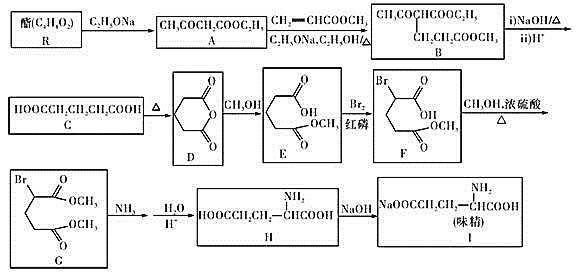
请回答下列问题:
![]() 下列有关蛋白质和氨基酸的说法不正确的是________
下列有关蛋白质和氨基酸的说法不正确的是________![]() 填字母代号
填字母代号![]() 。
。
![]() 蛋白质都是高分子化合物
蛋白质都是高分子化合物
![]() 谷氨酸
谷氨酸![]() 自身不能发生反应
自身不能发生反应
![]() 氨基酸和蛋白质都能发生盐析
氨基酸和蛋白质都能发生盐析
![]() 天然蛋白质水解的最终产物都是
天然蛋白质水解的最终产物都是![]() 氨基酸
氨基酸
![]() 的系统命名是________;F中含氧官能团的名称是_______________。
的系统命名是________;F中含氧官能团的名称是_______________。
![]() 的反应类型是____________,R的结构简式为_______________。
的反应类型是____________,R的结构简式为_______________。
![]() 写出G和
写出G和![]() 反应的化学方程式:_________________。
反应的化学方程式:_________________。
![]() 是H的同分异构体,T中同时具备下列条件的结构有________种。其中在核磁共振氢谱上有4组峰且峰的面积比为
是H的同分异构体,T中同时具备下列条件的结构有________种。其中在核磁共振氢谱上有4组峰且峰的面积比为![]() 的可能结构简式为_______。
的可能结构简式为_______。
![]() 能发生水解反应
能发生水解反应
![]() 只有2种官能团,其中一种是
只有2种官能团,其中一种是![]()
![]() 发生银镜反应能生成
发生银镜反应能生成![]() 银
银
![]() 参照上述流程,以
参照上述流程,以![]() 和甲醇为原料
和甲醇为原料![]() 其他无机试剂任选
其他无机试剂任选![]() ,设计合成苯丙氨酸
,设计合成苯丙氨酸![]()
![]() 的流程:_____________________。
的流程:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将0.1 mol/L的NaOH溶液滴入盛有50 mLpH=2 的HA溶液的绝热容器中,加入NaOH溶液的体积V与溶液温度T的关系如图。下列说法正确的是( )
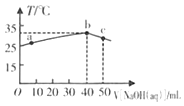
A.a点溶液中,c(A-)+c(HA)=0.08 mol/L
B.b点溶液中,c(A-)<c(Na+)
C.a→b的过程中,发生了吸热反应
D.溶液中HA的电离平衡常数a点等于b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫的催化氧化原理为2SO2(g)+O2(g)![]() 2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
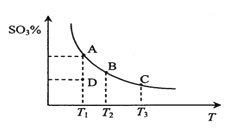
A. 反应2SO2(g)+O2(g)![]() 2SO3(g)的△H<0
2SO3(g)的△H<0
B. 在D点时v(正)<v(逆)
C. 若B、C点的平衡常数分别为KB、KC,则KB>KC
D. 恒温恒压下向平衡体系中通入氦气,平衡向左移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com