
已知热化学方程式H2(g)+F2(g)═2HF(g)△H=﹣270kJ•mol﹣1,下列说法中错误的是( )
|
| A. | 在上述条件下,44.8L氟化氢气体分解成22.4L氢气与22.4L氟气吸收270kJ热量 |
|
| B. | 在上述条件下,1mol氢气与1mol氟气反应生成2mol液态氟化氢放出热量大于270kJ |
|
| C. | 在上述条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量 |
|
| D. | 上述热化学方程式还可表示为: |
| 反应热和焓变;热化学方程式. | |
| 专题: | 化学反应中的能量变化. |
| 分析: | A、由热化学方程式可知2mol氟化氢气体分解成1mol的氢气和1mol的氟气吸收270kJ热量; B、液态氟化氢的能量比气态氟化氢的能量低,根据反应热与能量关系判断; C、反应物总能量大于生成物的总能量为放热反应,反应物总能量小于生成物的总能量为吸热反应; D、热化学方程式中化学计量数表示物质的量,不表示分子个数,系数改变焓变随之改变. |
| 解答: | 解:A、由热化学方程式可知2mol氟化氢气体分解成1mol的氢气和1mol的氟气吸收270kJ热量,化学计量数表示物质的量,不是体积,故A错误; B、液态氟化氢的能量比气态氟化氢的能量低,根据能量守恒,1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量大于270kJ,故B正确; C、反应为放热反应,在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量,故C正确; D、热化学方程式中化学计量数表示物质的量,计量数同时减小一倍,焓变也随之减小一倍,可表示为 故选:A. |
| 点评: | 本题考查学生对热化学方程式的理解、反应热与能量关系,难度不大,注意反应物总能量大于生成物的总能量为放热反应,反应物总能量小于生成物的总能量为吸热反应. |


科目:高中化学 来源: 题型:
某可逆反应从0~2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示。
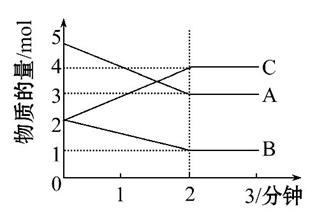
(1)该反应的反应物是 ,生成物是 。
(2)化学方程式为 。
(3)反应开始至2分钟时,能否用C表示反应速率?若能,其反应速率为 ,若不能,则其原因为 。
(4)2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达
到了 状态。
查看答案和解析>>
科目:高中化学 来源: 题型:
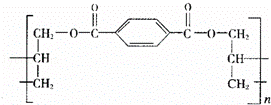
某种高分子化合物的结构简式如图所示:合成它的单位可能有:①对苯二甲酸,②对苯二甲酸甲酯,③丙烯醇,④丙烯,⑤乙烯.
其中正确的一组是( )
|
| A. | ①② | B. | ④⑤ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下用甲烷可以消除氮氧化物(NOx)的污染.已知:
①CH4( g )+4NO2( g )═4NO( g )+CO2( g )+2H2O( g )△H=﹣574kJ•mol﹣1
②CH4( g )+4NO( g )═2N2( g )+CO2( g )+2H2O( g )△H=﹣1160kJ•mol﹣1.
下列正确的选项是( )
|
| A. | CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(l)△H=﹣867kJ•mol﹣1 |
|
| B. | CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子总数为3.2mol |
|
| C. | 若0.2mol CH4还原NO2至N2,在上述条件下放出的热量为173.4kJ |
|
| D. | 若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为3.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中进行下列反应:2SO2(g)+O2(g)⇌2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol•L﹣1、0.1mol•L﹣1、0.2mol•L﹣1,当反应达到平衡时,可能存在的数据是( )
|
| A. | SO2为0.4mol•L﹣1,O2为0.2 mol•L﹣1 |
|
| B. | SO2为0.15 mol•L﹣1 |
|
| C. | SO2,SO3均为0.25 mol•L﹣1 |
|
| D. | SO3为0.4 mol•L﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分析如图所示的四个原电池装置,结论正确的是( )
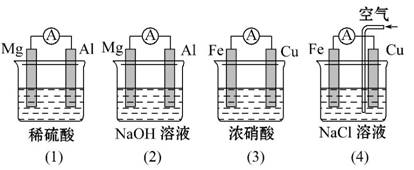
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为6H2O+6e-====6OH-+3H2↑
C.(3)中Fe作负极,电极反应式为Fe-2e-====Fe2+
D.(4)中Cu作正极,电极反应式为2H++2e-====H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
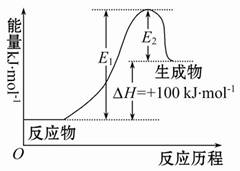
某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的是( )
A.正反应活化能小于100 kJ·mol-1
B.逆反应活化能一定小于100 kJ·mol-1
C.正反应活化能不小于100 kJ·mol-1
D.正反应活化能比逆反应活化能大100 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com