
【题目】农药波尔多液不能用铁制容器盛放,是因铁能与该农药中的硫酸铜起反应.在该反应中,铁是( )
A.氧化剂
B.还原剂
C.催化剂
D.漂白剂
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】下列事实能用同一原理解释的是:
A. SO2和Cl2都能用于漂白
B. I2、NH4Cl晶体受热都逐渐消失
C. 配制Fe(NO3)3和Sn(NO3)2溶液均要加入稀硝酸
D. SO2可使加酚酞的氢氧化钠溶液和酸性高锰酸钾溶液的红色都褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W 4种元素分别是元素周期表中3个连续短周期的元素且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)写出Z在周期表中的位置______________。W离子的结构示意图:_______________________。
(2)由以上元素中两两形成的化合物中,溶于水显碱性的气态氢化物的结构式为:__________________。
既含离子键又含非极性共价键的化合物的电子式为________;既含极性共价键又含非极性共价键的化合物的电子式为________。
(3)Z的氢化物熔沸点在其同主族氢化物中熔沸点最高,原因是_______________________。
(4)用化学方程式表示Z与其同主族短周期元素的非金属性强弱___________________________ 。
(5)由X、Y、Z所形成的常见离子化合物是________(写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为____________________;X与W形成的化合物与水反应时,水作________ (填“氧化剂”或“还原剂”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室进行下列实验,括号内的实验仪器或试剂都能用到的是
A.铝热反应(铝热剂、镁带、氯酸钾、蒸发皿)
B.钠的焰色反应(氯化钠溶液、盐酸、铂丝、蓝色钴玻璃)
C.中和热的测定(量筒、温度计、环形玻璃搅拌棒、酒精灯)
D.制取氢氧化铁胶体(饱和FeCl3溶液、NaOH溶液、烧杯、胶头滴管)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各图像的解释或结论正确的是( )
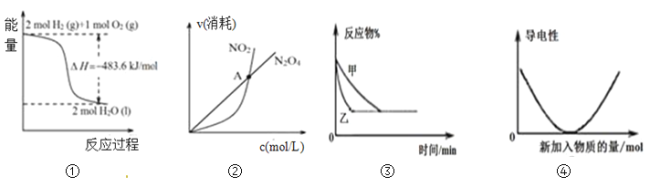
A.图①可知:热化学方程式是H2(g)+1/2O2(g)=H2O(g)△H=﹣241.8kJ/mol
B.图②可知:对于恒温恒容条件下的反应2NO2(g)![]() N2O4(g),A点为平衡状态
N2O4(g),A点为平衡状态
C.图③可表示:压强对2A(g)+2B(g)![]() 3C(g)+D(s)的影响
3C(g)+D(s)的影响
D.图④可表示:Ba(OH)2溶液中滴加稀硫酸,溶液导电性的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2A![]() B + D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
B + D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
实验 序号 | 浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800 | 1. 0 | 0.80 | 0.67 | 0.57 | 0.50 | c1 | 0.50 |
2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | T3 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据述数据,回答下列问题 :
(1)在实验1中,以反应物A浓度的变化表示该反应在0~10min内的平均反应速率为________ 。
(2)在实验1中,c1数值为 ________ 。
(3)在实验1、2中有一个实验使用了正催化剂。判断是实验 ________ (选填“1”或“2”)使用了正催化剂。
(4)在实验1、3中反应温度不同。判断T3 ________ 800(选填“﹤”或“﹥”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中表示碳原子相互结合的几种方式。小圆球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合,则下列说法正确的是
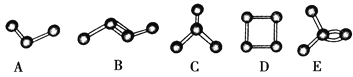
A. 图中属于烷烃的是A、C、D
B. 图中C和E分子中氢原子数相同
C. 图中物质碳元素的质量分数最小的是A
D. 图中与B互为同分异构体的有C、D、E
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应①X(g)+2Y(g) ![]() 2Z(g) 、②2M(g)
2Z(g) 、②2M(g)![]() N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
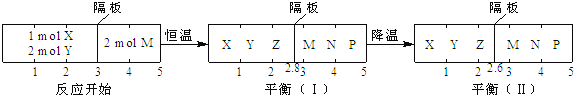
下列判断正确的是
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时,X的转化率为![]()
D.在平衡(I)和平衡(II)中M的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)浓硫酸与木炭粉在加热条件下的化学方程式为_____________________。
(2)已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是:
_____→_____→____→_____。(填装置的编号)

(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是_________,B瓶溶液的作用是_____________,C瓶溶液的作用是__________。
(4)装置②中所加的固体药品是_______________,可确证的产物是_______。
(5)装置③中所盛溶液是____________________,可验证的产物是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com