
| A. | CH3+和NH4+ | B. | OH-和NH2- | C. | NO2和NO3- | D. | CH4和Na |
分析 质子数等于原子的质子数之和,中性微粒中质子数等于电子数,阳离子的电子数等于质子数减去电荷数,而阴离子的电子数为质子数加电荷数.
解答 解:A.CH3+的质子数为9、电子数为8,NH4+的质子数为11、电子数为10,电子数目不同,故A错误;
B.OH-的质子数为9、电子数为10,NH2-的质子数为9、电子数为10,电子数目相同,故B正确;
C.NO2的质子数为23、电子数为23,NO3-的质子数为31、电子数为32,电子数目不同,故C错误;
D.CH4的质子数为10、电子数为10,Na的质子数为11、电子数为11,电子数目相同,故D错误;
故选B.
点评 本题考查微粒的质子数和电子数,明确质子数和电子数的计算及中性微粒中质子数等于电子数是解答本题的关键.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 与H2化合的能力:At2>I2 | B. | 砹在常温下为白色固体 | ||
| C. | 砹原子的最外层有7个电子 | D. | 砹易溶于水,难溶于四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
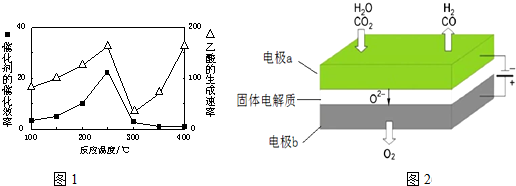
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在SiO2晶体中,由Si、O构成的最小单元环中共有8个原子 | |
| B. | 在28g晶体硅中,含Si-Si共价键个数为4NA | |
| C. | 金刚石的熔沸点高于晶体硅,是因为C-C键键能小于Si-Si键 | |
| D. | 镁型和铜型金属晶体的配位数均为12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2 NO H2O | B. | NaNO3 NaOH O2 H2O | ||
| C. | NaNO3 H2O | D. | NaNO3 HNO3 O2 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.5 mol | B. | 2 mol | C. | 1.25 mol | D. | 0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中滴加足量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| B. | 铜片与浓HNO3:Cu+2NO3-+2H+=Cu2++2NO2↑+H2O | |
| C. | NH4HCO3溶液与足量的NaOH溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 一水合氨的电离:NH3•H2O=NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 | |
| B. | 加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+$\frac{1}{2}$c(SO32-) | |
| C. | 加入少量NaOH溶液,$\frac{c(S{O}_{3}^{2-})}{c(HS{O}_{3}^{-})}$、$\frac{c(O{H}^{-})}{c({H}^{+})}$的值均增大 | |
| D. | 加入氨水至中性,则2c(Na+)=c(SO32-)>c(H+)=c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com