
| A. | ①②④ | B. | ①④ | C. | ①③ | D. | ①②③ |
分析 ①根据过渡元素金属离子对多种配体具有很强的结合力分析;
②配离子中中心原子提供空轨道,配体提供孤电子对;
③配合物中一定含有配位键;
④配位键不仅存在于配位化合物中,其它化合物中也可能有.
解答 解:①许多过渡元素金属离子对多种配体具有很强的结合力,因而过渡金属配合物远比主族金属的配合物多,故①正确;
②配离子中中心原子提供空轨道,配体提供孤电子对,所以[Cu(H2O)4]2+中的Cu2+提供空轨道,H2O中的O原子提供孤对电子,两者结合形成配位键,故②正确;
③所有的配合物中一定含有配位键,故③正确;
④配位键不仅存在于配位化合物中,其它化合物中也可能有,例如铵根离子中,故④错误;
故选D.
点评 本题考查了配合物的成键情况,题目难度中等,注意形成配合物的条件:有提供空轨道的中心原子,有提供孤电子对的配位体,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的醋酸的导电能力比纯醋酸的导电能力弱 | |
| B. | PH均为5的盐酸和NH4Cl溶液中水电离出来的c(H+)均为1×10-5mol•L-1 | |
| C. | PH=8.3的NaHC03溶液中:c(Na+)>c(HCO3- )>c(CO32-)>c(H2CO3) | |
| D. | 向0.10mol•L-1 NaHSO3溶液中通入NH3至溶液的PH=7,此时溶液中:c(Na+)>c(SO32-)>c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
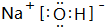 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8 g 2H2O所含中子总数为NA | |
| B. | 1 L 1 mol/L的甲醇水溶液中含有氢原子总数为4NA | |
| C. | 12g石墨和C60的混合物中质子总数为6NA | |
| D. | 反应KIO3+6HI═KI+3H2O+3I2中,生成1mol I2转移电子的总数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$、K+ | B. | K+、Cl-、Na+、SO${\;}_{4}^{2-}$ | ||
| C. | Mg2+、NO${\;}_{3}^{-}$、K+、Cl- | D. | Na+、Ba2+、Ca2+、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com