
| 实验 序号 | 加热前的质量 | 加热后的质量 | 失水质量 | 结晶水的值 | |
| m0(容器) | m1(容器+晶体) | m2(容器+无水硫酸铜) | |||
| 1 | 35.503g | 35.685g | 35.620g | ①0.065 | ②4.9 |
| 2 | 35.503g | 35.663g | 35.606g | ③0.057 | ④3.2 |
分析 (1)根据结晶水合物中,结晶水的质量=m(容器十晶体)-m(容器十无水硫酸铜),据化学方程式可以计算结晶水x的值;根据胆矾中结晶水为5计算出相对误差;
(2)实验结果偏低,在测定中若被测样品中含有加热不挥发的杂质或实验前被测样品已有部分失水,都会造成测量结果偏低.
解答 解:(1)实验1:坩埚的质量m0=35.503g、坩埚和胆矾的质量m1=35.685g、坩埚和硫酸铜的质量m2=35.620g,
胆矾的质量为:35.685g-35.503g=0.182g,
无水硫酸铜的质量为:35.620g-35.503g=0.117g,硫酸铜的物质的量为:$\frac{0.117g}{160g/mol}$=0.00073125mol,
结晶水的质量为:0.182g-0.117g=0.065g,结晶水的物质的量为:$\frac{0.065g}{18g/mol}$≈0.003611mol,
该胆矾中含有结晶水的数目为:$\frac{0.003611}{0.00073125}$≈4.9,
实:2:坩埚的质量m0=35.503g、坩埚和胆矾的质量m1=35.663g、坩埚和硫酸铜的质量m2=35.606g,
胆矾的质量为:35.663g-35.503g=0.16g,
无水硫酸铜的质量为:35.606g-35.503g=0.103g,硫酸铜的物质的量为:$\frac{0.16g}{160g/mol}$=0.001mol,
结晶水的质量为:0.16g-0.103g=0.057g,结晶水的物质的量为:$\frac{0.057g}{18g/mol}$≈0.00317mol,
该胆矾中含有结晶水的数目为:$\frac{0.00317}{0.001}$≈3.2,测得平均结晶水x=$\frac{3.2+4.9}{2}$≈4.1,
胆矾中含有5个结晶水,则该实验的相对误差为:$\frac{5-4.1}{5}×$100%=18%,
故答案为:0.065;4.9;0.057;3.2;4.1;18;
(2)A.加热前所用的坩埚未完全干燥.加热后水挥发,导致水的质量测定结果偏大,故A错误;
B.加热过程中晶体有少量溅失,导致质量差值偏大,测定结果偏大,故B错误;
C.加热后容器未放入干燥器中冷却,硫酸铜吸水,导致测定结果偏小,故C正确;
D.硫酸铜晶体中含有不分解失重的杂质,会导致计算所得硫酸铜晶体物质的量偏大,会造成测量结果偏低,故D正确;
故选CD.
点评 本题考查了实验室测定硫酸铜晶体结晶水含量实验,对失水得到产物的分析判断以及对实验结果产生的误差的原因进行分析是解答的关键,题目难度中等.


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶液中肯定不存在的离子只有Cu2+ | B. | Fe3+和Cu2+均完全被铁粉还原 | ||
| C. | 滤液中滴加KSCN溶液显红色 | D. | 滤渣中肯定不含有铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2溶液与Na2CO3溶液加足量稀醋酸 | |
| B. | Ba(OH)2溶液与KNO3溶液加足量H2SO4 | |
| C. | AgNO3溶液与Na2CO3溶液加足量稀硝酸 | |
| D. | Ca(OH)2溶液与FeCl3溶液加足量稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
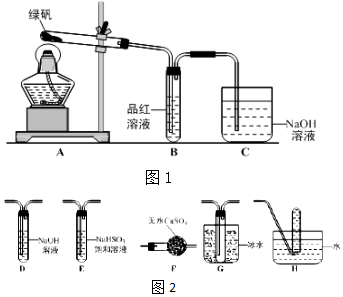
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅在地壳中含量丰富,广泛用于制造水泥、玻璃、陶瓷等 | |
| B. | 硅酸钠在建筑工业上常用作黏合剂和木材防火剂 | |
| C. | 碳化硅的结构与金刚石相似,硬度很大常用做砂轮和砂纸 | |
| D. | 硅是良好的半导体材料故用作光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度可增大单位体积活化分子数百分数,促进有效碰撞,从而提高反应速率 | |
| B. | 增大体系压强可增大单位体积活化分子数,促进有效碰撞,从而提高反应速率 | |
| C. | 放热反应(△H<0)和熵增(△S>0)反应一定能自发反应 | |
| D. | 由能量守恒可知任何放热反应都可设计成原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com