
����Ŀ��һ���¶��£����ݻ�Ϊ2 L���ܱ�������Ͷ��һ����M��N���з�Ӧ��M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ��
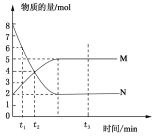
��1��д���˷�Ӧ�Ļ�ѧ����ʽ________________________��
��2��������������˵��������Ӧ�ﵽƽ��״̬����_____��
A����Ӧ��M��N�����ʵ���֮��Ϊ1:1
B���ڻ��������N�������ٷ������ֲ���
C����������ƽ��Ħ����������ʱ��ı仯���仯
D����������ѹǿ����ʱ��ı仯���仯
��3����t3=3����3min����M��ʾ�ķ�Ӧ������ ��
��4����t2ʱ������Ӧ����v���������淴Ӧ����v���棩�Ĵ�С��ϵ�� ��
��5����Ӧ�ﵽƽ���N��ռ����������� ������һλС������
��������1�� 2N(g)![]() M(g) ��2��BCD(2������һ����1������һ�����÷�)��3��0.5mol/��L��min������д��λ��1�֣���4��v�������� v���棩(1��) ��5��28.6%
M(g) ��2��BCD(2������һ����1������һ�����÷�)��3��0.5mol/��L��min������д��λ��1�֣���4��v�������� v���棩(1��) ��5��28.6%
��������
�����������1����ʱ����У�N�����ʵ�����С��N����Ӧ���������N�����ʵ���Ϊ��ֵ�Ҳ�Ϊ�㣬��ӦΪ���淴Ӧ������n��N������n��M��=��8-2��mol����5-2��mol=2��1���������仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪��Ӧ�Ļ�ѧ����ʽΪ2N(g)![]() M(g)��
M(g)��
��2��A��ƽ��ʱ��Ӧ��������ֵ����ʵ������䣬������ֵ����ʵ�����һ����ȣ�A����B������Ӧ�ﵽƽ��״̬ʱ�������ʵ�Ũ�ȡ��������ٸı䣬���������N�������ٷ������ֲ��䣬˵������ƽ�⣬B��ȷ��C���淴Ӧ���л�����������ʵ��������仯����������ƽ����Է��Ӳ���ʱ��ı仯���仯��˵�������ʵ������䣬˵����ƽ�⣬C��ȷ��D���淴Ӧ���л�����������ʵ��������仯����������ѹǿ����ʱ��ı仯���仯���������������ʵ�������ʱ��ı仯���仯��˵������ƽ�⣬D��ȷ����ѡBCD��
��3������v=��c����t��֪����t3=3����3min����M��ʾ�ķ�Ӧ����v=![]() =0.5mol/��Lmin����
=0.5mol/��Lmin����
��4��t2ʱ�̣�����ͼ��N�����ʵ���������С��M�����ʵ����������ж���Ӧ������У���v��������v���棩��
��5���������֮��=���ʵ���֮�ȣ�����ͼ��������Ӧ�ﵽƽ���N��ռ���������=![]() ��100%
��100%
=28.6%��


 ��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д�
��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д� ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩΪԭ�Ϻϳɻ�״������ E(C4H4O4)���������¡�
![]()
��ش��������⣺
��1��E �Ľṹ��ʽ��_______________��C �����������ŵ�������____________��
��2������ϩ��ͬϵ���У�����̼ԭ��һ����ƽ����̼ԭ�������ķ��ӵĽṹ��ʽ��__________������(ϵͳ����)��______________��
��3����Ӧ�����У�����ȡ����Ӧ����_______(��д���)��
��4��д����Ӧ���Ļ�ѧ����ʽ______________ ��
��5��F��E��ͬ���칹�壬��1 mol F�������� NaHCO3��Һ��Ӧ�ɷų�2mol CO2���壬��д������������F�����еĽṹ��ʽ______________ ��
��6�����������ϳ�·�ߵı�ʾ���������ϩΪԭ���Ʊ��Ҷ��������ϳ�·�ߣ�
__________________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ������С��36��X��Y��Z��W����Ԫ�أ�����X�������к�������Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�W��+1�������ӵĺ�����3�����Ӳ��Ҹ����������
�ش��������⣺
��1��W+�ļ۵����Ų�ʽΪ ��
��2��Y2X2������Yԭ�ӹ�����ӻ�����Ϊ ��1mol Y2X2������������ĿΪ ��
��3��������ZX3�ķе�Ȼ�����YX4�ĸߣ�����Ҫԭ���� ��
��4��Ԫ��Y��һ����������Ԫ��Z��һ�������ﻥΪ�ȵ����壬Ԫ��Z������������ķ���ʽ�� ��
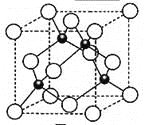
��5��Ԫ��W��һ���Ȼ��ᄃ��ľ����ṹ��ͼ��ʾ�����Ȼ���Ļ�ѧʽ�� ��������Ũ���ᷢ����������ԭ��Ӧ�����������H2WCl3����Ӧ�Ļ�ѧ����ʽΪ ���ھ����������2��ԭ�Ӿ�����apm���������ܶ���_____________g��cm-3(ֻҪ������ʽ�����ؼ������ֵ������٤������ΪNA)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(CH3OCH3)��һ��������Դ�����ö�����̼�ϳ�����Դ�ѳ�Ϊ������ѧ���о������ſ��⡣
��1�����ֹ��ۼ��ļ��������ʾ��
��ѧ�� | C=O | H-H | C-H | C-O | H-O |
����/kJ��mol-1 | 803 | 436 | 414 | 326 | 464 |
2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ![]() _______________��
_______________��
��2�����˹�������á�����������Ŀ���ü���ģ������Ĺ�����ã�����̫���⽫H2O��CO2ֱ�Ӻϳ�ȼ�Ϻͻ���ԭ�ϡ�������Աģ�������ã������ͼ����ʾװ���Ʊ������ѡ�����ת����ʽΪ̫����![]() ����
����![]() ��ѧ�ܡ�
��ѧ�ܡ�
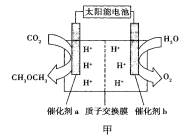
������b�ĵ缫������_________________��
�����ͷ�11.2L��������״���£�����___________mol H+___________�������ӵ�Ǩ�Ʒ���
������a�ϵĵ缫��ӦʽΪ______________��
��3����ʢ�ٴ�ѧ���о���Ա�о���һ�ַ�������ʵ��ˮ������ʱCO2�����ŷţ������ԭ����ͼ����ʾ��
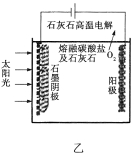
������������������ת����ʽ��__________________��
����ⷴӦ���¶�С��900![]() ʱ���У�̼��Ʒֽ�ΪCaO��CO2�������Ϊ����̼���ƣ��������ĵ缫��ӦʽΪ_______________�������ĵ缫��ӦʽΪ______________��
ʱ���У�̼��Ʒֽ�ΪCaO��CO2�������Ϊ����̼���ƣ��������ĵ缫��ӦʽΪ_______________�������ĵ缫��ӦʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���H����Na����NH4+��Fe3����Al3����SO![]() ��CO
��CO![]() �����ӡ��������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ������ʵ�����NaOH��Һ����仯��ͼ����ͼ��ʾ������˵����ȷ������ ��
�����ӡ��������Һ�м���һ�����ʵ���Ũ�ȵ�NaOH��Һʱ���������ɳ������ʵ�����NaOH��Һ����仯��ͼ����ͼ��ʾ������˵����ȷ������ ��
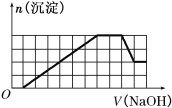
A��ԭ��Һ�к��е���������H����Fe3����Al3��
B��ԭ��Һ��һ������SO![]() ��Na��
��Na��
C��ԭ��Һ�к��е�Fe3����Al3�������ʵ���֮��Ϊ1��1
D����Ӧ����γɵ���Һ�к��е�����ΪNa2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
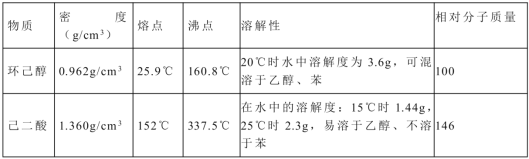
����Ŀ��������![]() ��һ�ֹ�ҵ�Ͼ�����Ҫ������л���Ԫ�ᣬ�ڻ����������л��ϳɹ�ҵ��ҽҩ��������ȷ��涼����Ҫ���ã��ܹ��������η�Ӧ���ữ��Ӧ�ȣ��������Ԫ�����۳ɸ߷��Ӿۺ���ȣ���������������ж�Ԫ�����еĵڶ�λ��ʵ���Һϳɼ�����ķ�Ӧԭ����ʵ��װ��ʾ��ͼ���£�
��һ�ֹ�ҵ�Ͼ�����Ҫ������л���Ԫ�ᣬ�ڻ����������л��ϳɹ�ҵ��ҽҩ��������ȷ��涼����Ҫ���ã��ܹ��������η�Ӧ���ữ��Ӧ�ȣ��������Ԫ�����۳ɸ߷��Ӿۺ���ȣ���������������ж�Ԫ�����еĵڶ�λ��ʵ���Һϳɼ�����ķ�Ӧԭ����ʵ��װ��ʾ��ͼ���£�![]()
�����õ����й��������£�
ʵ�鲽�����£�
������������ƿ�м���16mL 50%�����ᣨ�ܶ�Ϊ1.31g/cm�����ټ���1��2����ʯ����Һ©����ʢ����5.4mL��������
����ˮԡ����������ƿ��50�����ң���ȥˮԡ�������μ�5��6�λ�������ҡ��������ƿ���۲쵽�к���ɫ����ų�ʱ�������μ�ʣ�µĻ�������ά�ַ�Ӧ�¶���60����65 ��֮�䡣
������������ȫ��������������80��-90��ˮԡ����Լ10min��ע������¶ȣ���ֱ������ɫ��������Ϊֹ��
�������Ƚ���ӦҺ�����ձ��У������ˮԡ����ȴ�������������ˡ�ϴ�ӵôֲ�Ʒ��
�����ֲ�Ʒ���ᴿ�����Ϊ5.7g��
��ش��������⣺
��1����Һ©����ϸ֧��a��������________������b������Ϊ________��
��2����֪��NaOH��Һ����β��ʱ��������ط�Ӧ����ʽΪ��2NO2+2NaOH=NaNO2 +NaNO3 +H2O
NO+NO2+2NaOH =2NaNO2+H2O��������ô�����Һ����β��ʱҲ�ܷ������Ʒ�Ӧ������ط�Ӧ����ʽΪ��_________________��__________________��
��3����������ƿ�еμӻ�����ʱ��Ҫ���ƺû������ĵ������ʣ���ֹ��Ӧ���ھ��ҵ����¶�Ѹ�����������������ɽ����صĺ�������о�һ�����ܲ����ĺ����_________________________________��
��4��Ϊ�˳�ȥ���ܵ����ʺͼ��ٲ�Ʒ��ʧ���ɷֱ��ñ�ˮ��________ϴ�Ӿ��塣
��5���ֲ�Ʒ����________���ᴿ(��ʵ���������)����ʵ�����õ��ļ��������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ǹ�ϰ�˳����ļ��ֽ�����Na��Mg��Al��Fe��Cu������������ѧ֪ʶ�ش��������⣺
��1����ԭ�Ӻ��������________�˶�״̬���仯����Na2O2������________________��
��2��þ�ڶ�����̼�е�ȼ�Ļ�ѧ����ʽΪ______________________________��
��3������Ԫ�����ڱ���λ��______________________________��
��4����ȥFe�е�����Al��������Ӧ�����ӷ���ʽΪ_____________________________��
��5�����漸�ֽ����п����Ȼ�ԭ��ұ������______________________________��
��6��ͭ�ļ۵����Ų�ʽΪ3d104s1������3d94s2������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�����ö�������(CeO2)��̫���������½�H2O��CO2ת���H2��CO����������£�mCeO2![]() (m-x)CeO2��xCe+xO2
(m-x)CeO2��xCe+xO2
(m-x)CeO2��xCe+xH2O+ xCO2![]() mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
����˵������ȷ����( )
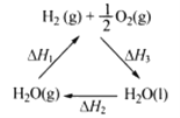
A���ù�����CeO2û������
B���ù���ʵ����̫������ѧ�ܵ�ת��
C����ͼ����H1=��H2+��H3
D����CO��O2���ɵļ���ȼ�ϵ�صĸ�����ӦʽΪCO+4OH����2e��=CO32-+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú���ۺ����ö��ڸ��ƴ�����������Դ�����������Ҫ�����塣
��1������˵����ȷ���� ������ţ���
a��ú�����л��������������ɵĸ��ӻ����
b��ú��ȼ�չ����л�����һ����̼��������̼����������̳����к�����
c����������ʯ�ҡ���ʯ�ҡ�ʯ��ʯ�ȹ����ʹú��ȼ�չ����������ȶ���������
d��ú�ĸ������ڻ�ѧ�仯��ú��������Һ�������������仯
��2��ú�����������в������к�����H2S�ð�ˮ�����������ε����ӷ���ʽ��
��
��3��ȼú������һ������-���-ʯ��-ʯ�෨����ͼ1���£�
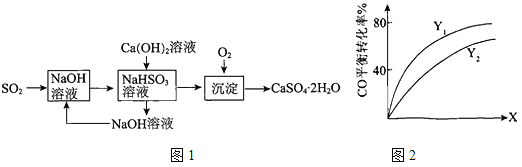
�������£���NaOH��Һ����SO2�õ�pH��6��NaHSO3��Һ������Һ������Ũ�ȵĴ�С˳����
��
������������NaHSO3��Ӧ�Ļ�ѧ����ʽ�� ��
��4��ú�ļ��Һ�����ϳɶ����ѵ�������Ӧ���£�
��2H2(g)+CO(g) ![]() CH3OH(g) ��H=-90.8kJ��mol-1
CH3OH(g) ��H=-90.8kJ��mol-1
��2CH3OH(g) ![]() CH3OCH3(g)+ H2O(g) ��H=-23.5 kJ��mol-1
CH3OCH3(g)+ H2O(g) ��H=-23.5 kJ��mol-1
��CO(g) + H2O(g) ![]() CO2(g) + H2(g) ��H=-41.3 kJ��mol-1
CO2(g) + H2(g) ��H=-41.3 kJ��mol-1
�� �ܷ�Ӧ�Ȼ�ѧ����ʽ��3H2(g)+ 3CO(g) ![]() CH3OCH3(g)+ CO2(g) ��H=
CH3OCH3(g)+ CO2(g) ��H=
�� Y��Y1��Y2����X�ɷֱ����ѹǿ���¶ȡ���ͼ2��ʾYһ��ʱ���ܷ�Ӧ��CO��ƽ��ת������X�ı仯��ϵ���ж�Y1��Y2�Ĵ�С��ϵ�����������ɣ�
��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com