
【题目】[选修3--物质结构与性质]M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子.元素Y的负一价离子的最外层电子数与次外层的相同.回答下列问题:
(1)单质M的晶体类型为 , 晶体中原子间通过作用形成面心立方密堆积,其中M原子的配位数为 .
(2)元素Y基态原子的核外电子排布式为 , 其同周期元素中,第一电离能最大的是(写元素符号).元素Y的含氧酸中,酸性最强的是(写化学式),该酸根离子的立体构型为 .
(3)M与Y形成的一种化合物的立方晶胞如图所示.
①该化合物的化学式为 , 已知晶胞参数a=0.542nm,此晶体的密度为gcm﹣3 . (写出计算式,不要求计算结果.阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是 . 此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为 .
【答案】
(1)金属晶体;金属键;12
(2)1s22s22p63s23p5;Ar;HClO4;正四面体
(3)CuCl;![]() ;Cu+可与氨形成易溶于水的配位化合物;[Cu(NH3)4]2+
;Cu+可与氨形成易溶于水的配位化合物;[Cu(NH3)4]2+
【解析】解:(1)铜属于金属,金属阳离子与电子之间通过金属键结合在一起,晶体类型为金属晶体,铜晶体是面心立方堆积,采用沿X、Y、Z三轴切割的方法知,每个平面上铜原子的配位数是4,三个面共有4×3=12个铜原子;所以答案是:金属晶体;金属键;12;
(2)元素氯是17号元素,位于第三周期,依据构造原理其基态电子排布为:1s22s22p63s23p5;其同周期元素中,第一电离能最大的是Ar,含氯的酸中高氯酸酸性最强是含有酸中最强酸,化学式为:HClO4 , 高氯酸酸根离子中氯原子为sP3杂化,没有孤对电子数,立体构型为正四面体;
所以答案是:1s22s22p63s23p5;Ar;HClO4; 正四面体;
(3)①依据晶胞结构,利用切割法分析,每个晶胞中含有铜原子个数为:8× ![]() +6×
+6× ![]() =4,氯原子个数为4,则化学式为;CuCl;1mol晶胞中含有4molCuCl,1mol晶胞的质量为M(CuCl)×4,晶胞参数a=0.542nm,则晶体密度为
=4,氯原子个数为4,则化学式为;CuCl;1mol晶胞中含有4molCuCl,1mol晶胞的质量为M(CuCl)×4,晶胞参数a=0.542nm,则晶体密度为 ![]() ;所以答案是:CuCl;
;所以答案是:CuCl; ![]() ;
;
②Cu+可与氨形成易溶于水的配位化合物,所以CuCl难溶于水但易溶于氨水;该化合物中Cu+被氧化为Cu2+ , 所以深蓝色溶液中阳离子为:[Cu(NH3)4]2+;所以答案是:Cu+可与氨形成易溶于水的配位化合物(或配离子);[Cu(NH3)4]2+ .


科目:高中化学 来源: 题型:
【题目】自来水可用氯气消毒,某学生用这种自来水去配制下列物质溶液,会产生明显的药品变质问题的是
A. NaNO3 B. FeCl2 C. Na2SO4 D. AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为探究影响过氧化氢分解的因素,做了三个实验。相应的实验结果如下图所示,请分析回答:
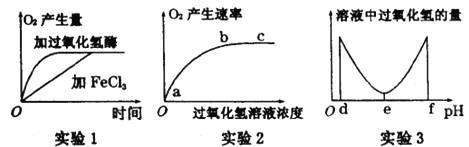
(1)实验1、2、3中的自变量分别为 。
(2)实验1的目的是探究 。
(3)实验2探究了过氧化氢溶液的浓度对过氧化氢酶的影响,该实验的结果显示 ,be段O2产生速率不再增大的原因最可能是 。
(4)实验3的结果显示,过氧化氢酶的最适pH为 。实验还证实,当pH小于d或大于f时,过氧化氢酶的活性将永久丧失,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是
A.将FeCl3溶于盐酸配制FeCl3溶液
B.加热稀醋酸溶液其pH降低
C.用低浓度铁盐溶液获得纳米氧化铁
D.小苏打溶液与AlCl3溶液混合产生气体和沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,下列描述不正确的是( )
A.C的成分是气体E与二氧化碳的混和气体
B.浓热的D溶液能把碳单质氧化为二氧化碳
C.气体E遇空气会被氧化成红棕色的气体
D.溶液G是蓝色的硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制100mL 0.1mol/L Na2SO4溶液,正确的方法是( ) ①将32.2g Na2SO4 . 10H2O溶于少量水中,再加水稀释至100mL
②将14.2g Na2SO4溶于100mL水中
③将20mL 0.5mol/L Na2SO4溶液用水稀释至100mL.
A.①②
B.②③
C.①③
D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示构成细胞的元素及其有不同有机化合物,a、b、c、d代表不同的小分子物质,A、B、C代表不同的大分子物质,请分析并回答下列问题:

(1)若A为植物细胞特有的储能物质,则A为__,在动物细胞内,与物质A作用最相近的是__。
(2)若物质A 在动植物细胞中均可含有,并且作为细胞内最理想的储能物质,则A是__。物质b的分子结构式__,鉴定物质B的试剂使用方法是__。
(3)物质c在动物细胞中共有__种,分子中__的不同决定了c的种类不同.物质d是__,它属于固醇类物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠单质性质的叙述中不正确的是( )
A. 在空气中极易被氧化,常保存在煤油中
B. 是一种银白色金属,具有金属光泽
C. 能与氯化铜溶液反应生成氯化钠和铜
D. 在空气中燃烧火焰为黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)[探究一]将已除去表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移人硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y.
①甲同学认为X中除Fe3+外还可能含有Fe2+ . 若要确认其中的Fe2+ , 应选用(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O═2HBr+H2SO4
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g.由于此推知气体Y中SO2的体积分数为
(3)[探究二]分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和Q气体.为此设计了下列探究实验装置(图中夹持仪器省略). 
装置B中试剂的作用是 .
(4)认为气体Y中还含有Q的理由是(用化学方程式表示).
(5)为确认Q的存在,需在装置中添加M于(选填序号).
a.A之前 b.A﹣B间 c.B﹣C间 d.C﹣D间
(6)如果气体Y中含有H2 , 预计实验现象应是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com