


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
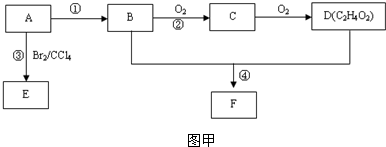
查看答案和解析>>
科目:高中化学 来源: 题型:

 +CH3CH2OH→
+CH3CH2OH→ +HCl,写出草酰氯(分子式C2O2Cl2,分子结构式:
+HCl,写出草酰氯(分子式C2O2Cl2,分子结构式: )与足量有机物D反应的最终化学方程式
)与足量有机物D反应的最终化学方程式 ,由邻甲基苯酚--中间产物--有机物A,请选择正确中间产物(填B或C)
,由邻甲基苯酚--中间产物--有机物A,请选择正确中间产物(填B或C) C:
C:
查看答案和解析>>
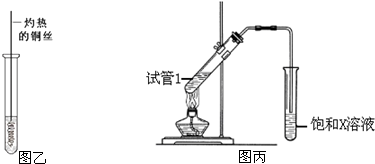
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:
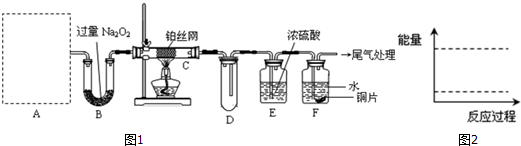
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| HCN | S8 | SF6分子 | B12结构单元 | |
| 结构模型示意图 |  |  |  |  |
| 备注 | / | 易溶于CS2 | / | 熔点1873K |
| A、HCN的结构式为H-C≡N |
| B、固态硫S8属于原子晶体 |
| C、SF6是由极性键构成的非极性分子 |
| D、单质硼属原子晶体,结构单元中含有30个B-B键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 .有机物X的键线式为:
.有机物X的键线式为: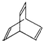
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com