已知可逆反应:M(g)+N(g)?P(g)+Q(g)△H>0,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为c(M)=1mol?L
-1,c(N)=2.4mol?L
-1;达到平衡后,M的转化率为60%,此时N的转化率为
;
(2)若反应温度升高,M的转化率
(填“增大”、“减小”或“不变”);
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4mol?L
-1,c(N)=a mol?L
-1;达到平衡后,c(P)=2mol?L
-1,a=
;
(4)若反应温度不变,反应物的起始浓度为c(M)=c(N)=b mol?L
-1,达到平衡后,M的转化率为
.(已知√0.5=0.5)
(5)T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T
1和T
2时,Y的体积百分含量与时间的关系如图2所示.则下列结论正确的是
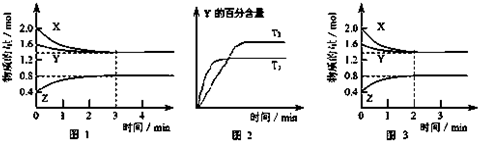
A.容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g)
B.反应进行的前3min内,用X表示的反应速率 v(X)=0.3mol/(L?min)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强.




 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案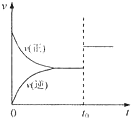 可逆反应aX(g)+b Y(g)?cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(u)一时间(t)图象如图.则下列说法中正确的是( )
可逆反应aX(g)+b Y(g)?cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(u)一时间(t)图象如图.则下列说法中正确的是( )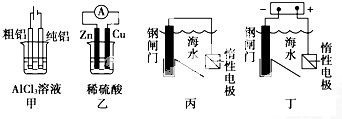
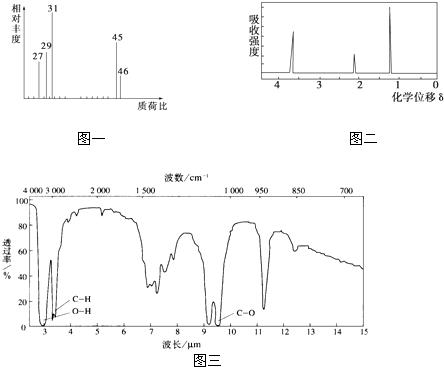
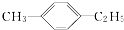 与苯为同系物,但
与苯为同系物,但 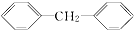 与苯不是同系物
与苯不是同系物