
 ,Z元素在周期表中的位置为第三周期第ⅥⅠA族族,能否用下面的反应证明Z的非金属性比碳强:2HCl+Na2CO3=NaCl+H2O+CO2↑否(填“能”或“否”)
,Z元素在周期表中的位置为第三周期第ⅥⅠA族族,能否用下面的反应证明Z的非金属性比碳强:2HCl+Na2CO3=NaCl+H2O+CO2↑否(填“能”或“否”) 分析 三种元素分别为H、Na、Cl的三种元素X、Y、Z两两组合的化合物HCl含有的化学键类别为共价键,氯化钠是离子化合物,是钠离子和氯离子通过静电作用形成的,其电子式为 ;氯是三个周期,最外层7个电子,所以在周期表中的位置为第三周期第ⅥⅠA族,反应2HCl+Na2CO3=NaCl+H2O+CO2↑只能说明盐酸的酸性强于碳酸,盐酸是无氧酸,而碳酸是含氧酸,应通过比较最高价含氧酸的酸性,得出两者的非金属性强弱,由此分析解答.
;氯是三个周期,最外层7个电子,所以在周期表中的位置为第三周期第ⅥⅠA族,反应2HCl+Na2CO3=NaCl+H2O+CO2↑只能说明盐酸的酸性强于碳酸,盐酸是无氧酸,而碳酸是含氧酸,应通过比较最高价含氧酸的酸性,得出两者的非金属性强弱,由此分析解答.
解答 解:三种元素分别为H、Na、Cl的三种元素X、Y、Z两两组合的化合物HCl含有的化学键类别为共价键,氯化钠是离子化合物,是钠离子和氯离子通过静电作用形成的,其电子式为 ;氯是三个周期,最外层7个电子,所以在周期表中的位置为第三周期第ⅥⅠA族,反应2HCl+Na2CO3=NaCl+H2O+CO2↑只能说明盐酸的酸性强于碳酸,而不能证明氯的非金属性比碳强,故答案为:共价键;
;氯是三个周期,最外层7个电子,所以在周期表中的位置为第三周期第ⅥⅠA族,反应2HCl+Na2CO3=NaCl+H2O+CO2↑只能说明盐酸的酸性强于碳酸,而不能证明氯的非金属性比碳强,故答案为:共价键; ;三;ⅥⅠA族;否.
;三;ⅥⅠA族;否.
点评 本题考查元素在周期表中的位置及性质递变规律和酸性比较等知识,侧重于学生的分析能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2017届湖北省荆门市高三上九月联考化学试卷(解析版) 题型:选择题
下列离子组在一定条件下能大量共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO3-、K+ | 稀硫酸 | 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-=Fe(OH)3↓ |
C | Ba2+、HCO3-、Cl- | 氢氧化钠溶液 | HCO3-+ OH-=CO32-+H2O |
D | Al3+、Cl-、NO3- | 过量氢氧化钠溶液 | Al3++3 OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上第二次月考化学试卷(解析版) 题型:选择题
1 mol Na2O2晶体和1 mol Na2O的晶体中阴离子的个数比较,前者和后者的关系是( )
A.前者大 B.前者小 C.相等 D.不能肯定
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管、碱式滴定管及锥形瓶均需洗净后再润洗内壁2-3次 | |
| B. | 可使用酚酞或甲基橙作指示剂 | |
| C. | 滴定过程中眼睛应始终注视滴定管内液面变化 | |
| D. | 读取标准溶液的刻度时,滴定前平视,滴定后仰视,测定结果偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 和
和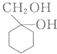 的流程路线.
的流程路线.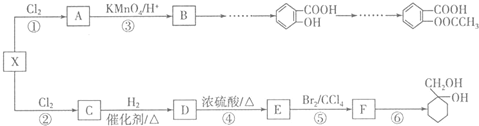
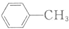 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$
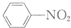 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$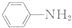 (苯胺,易被氧化)
(苯胺,易被氧化)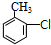 .
.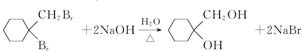 .
. 有多种同分异构体,写出符合下列条件的同分异构体的结构简式
有多种同分异构体,写出符合下列条件的同分异构体的结构简式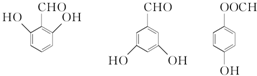 (任写一种).
(任写一种).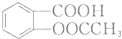 的结构与性质,说法正确的是AD.
的结构与性质,说法正确的是AD.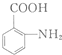 最合理的方案,请在答题纸的方框中表示.
最合理的方案,请在答题纸的方框中表示.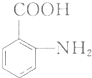
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | O=O | C-O | O-H | C-H |
| 键能(kJ•mol-1) | 498 | 351 | 465 | 413 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
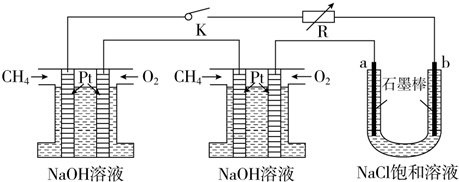
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com