
科目:高中化学 来源: 题型:阅读理解
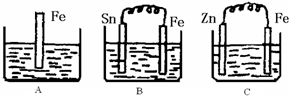
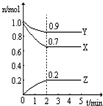
 2Z
2Z 2Z
2Z查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
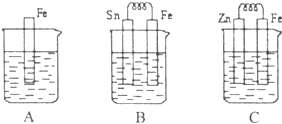 I.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
I.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(X-)>c(Y-) | B、电离程度:HX>HY | C、HY溶液的pH值>HX溶液的pH | D、HY溶液中的c(H+)>HX溶液中的c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用沸点数据推测两种液体混合物用蒸馏方法分离开来的可能性 | B、用几种一元弱酸的电离常数Ka来比较相同温度下相同物质的量浓度的这几种一元弱酸的钠盐溶液的碱性强弱 | C、用几种相同类型的难溶电解质的Ksp来比较相同温度下它们的溶解度的大小 | D、用熔、沸点数据来分析分子的稳定性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com