
 Fe3O4+4H2.该反应中氧化剂是________(填化学式,下同),还原剂是________.若消耗了1.5mol Fe,则生成________mol H2.
Fe3O4+4H2.该反应中氧化剂是________(填化学式,下同),还原剂是________.若消耗了1.5mol Fe,则生成________mol H2. 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2AlN+3CO.该反应中每生成2mol AlN,N2得到______mol电子.
2AlN+3CO.该反应中每生成2mol AlN,N2得到______mol电子.查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 Si3N4+6CO.下列叙述正确的是
Si3N4+6CO.下列叙述正确的是查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
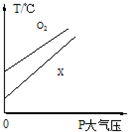 某同学进行实验时发现,在体积相等的两个恒容密闭容器中,分别充入等质量的某气体X和O2,测得温度与压强关系如图所示,请你判断下列说法正确的是
某同学进行实验时发现,在体积相等的两个恒容密闭容器中,分别充入等质量的某气体X和O2,测得温度与压强关系如图所示,请你判断下列说法正确的是查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com