
【题目】某有机物的分子式为C4H8O2,下列有关其同分异构体数目的说法中正确的是( )
A. 属于酯类的有4种
B. 属于羧酸的有3种
C. 既含有羟基又含有醛基的有3种
D. 不可能存在分子中含有六元环的同分异构体
【答案】A
【解析】A、C4H8O2属于酯类的同分异构体,为饱和一元酯,若为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇有2种,形成的酯有2种,若为乙酸与乙醇形成的酯,乙酸只有1种结构,乙醇只有1种结构,形成的乙酸乙酯有1种,若为丙酸与甲醇形成的酯,丙酸只有1种结构,甲醇只有1种结构,形成的丙酸甲酯只有1种,所以C4H8O2属于酯类的同分异构体共有4种,选项A正确;B、C4H8O2属于羧酸时,可以是丁酸或2-甲基丙酸,共有2种同分异构体,选项B错误;C、C4H8O2属于羟基醛时,可以是2-羟基丁醛、3-羟基丁醛、4-羟基丁醛、2-甲基-2-羟基丙醛、2-甲基-3羟基丙醛,共5种同分异构体,选项C错误;D、存在分子中含有六元环的同分异构体: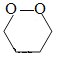 ,选项D错误。答案选A。
,选项D错误。答案选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】当物质发生化学反应时,断开反应物中的化学键要__________能量,而形成生成物中的化学键要__________能量,一个确定的化学反应的能量变化决定于反应物的总能量与生成物的总能量的相对大小。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两个体积相同的容器一个盛有CO2,另一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的()
A. 原子总数
B. 质子总数
C. 分子总数
D. 质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生如下反应:mA(g)+nB(g) ![]() pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
A. ![]() B. 平衡向逆反应方向移动
B. 平衡向逆反应方向移动
C. A的转化率减小 D. C的体积分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是 ( )

A. 31d和33d属于同种核素
B. 气态氢化物的稳定性:a>d>e
C. b、c、d、e四种元素中都存在能促进水的电离的含氧酸盐
D. e和其它四种元素均能形成共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。硫、氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要措施。
I.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1:3、3:1、4:1时,NO脱除率随温度变化的曲线如图所示。

(1)①曲线a中,NO的起始浓度为6×10-4mg/m3,从A 点到B点经过0.8 s,该时间段内NO的脱除速率为____________mg/(m3·s)。
②曲线b对应的NH3与NO的物质的量之比是____,其理由是___________________
(2)已知在25℃,101 kPa时:

请写出用NH3脱除NO的热化学方程式:____________________________________
Ⅱ.工业上还可以变“废”为“宝”,将雾霾里含有的SO2、NO等污染物转化为Na2S2O4(保险粉)和NH4NO3等化工用品,其生产流程如下图:

(3)装置Ⅱ中NO转变为NO3-的反应的离子方程式为__________________________________
(4)装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1 mol CH4 时,理论上可再生____mol Ce4+。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学选修-物质结构与性质】
已知前四周期六种元素A、B、C、D、E、F的原子序数之和为107,且它们的核电荷数依次增大,B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成A2C型离子化和物,其中的阴、阳离子相差一个电子层,E4+离子和氩原子的核外电子排布相同.请回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序是______(填元素符号)
(2)化合物BD3的分子空间构型可描述为______,B的原子轨道杂化类型为______。
(3)已知F元素在人体内含量偏低时,会影响O2在体内的正常运输.已知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物.则F的基态原子价电子排布式为______。CN-与______(一种分子)互为等电子体,则1个CN-中π键数目为______。
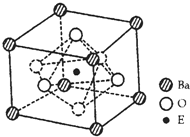
(4)EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为______,
在该晶体中,E4+的氧配为数为______。若该晶胞边长为anm可计算该晶体的密度为______g/cm3(阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
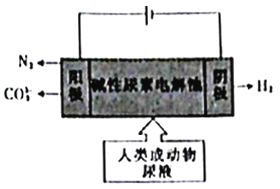
【题目】电解尿素[CO(NH2)2]是一种能耗很低的制氢方法,其工作原理如图所示,总反应为CO(NH2)2+2OH-![]() N2↑+3H2↑+CO32-。下列说法错误的是
N2↑+3H2↑+CO32-。下列说法错误的是
A. 阴极的材料可选择钢铁制品
B. 电解池工作时,阳极区域溶液的pH减小
C. 阳极的电极反应式为CO(NH2)2+8OH--6e-==N2↑+ CO32-+6H2O。
D. 若电路中通过3 mol 电子,则生成气体的总体积为33. 6L(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com