
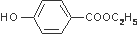
 ,其生产过程如图所示(反应条件未全部注明):
,其生产过程如图所示(反应条件未全部注明):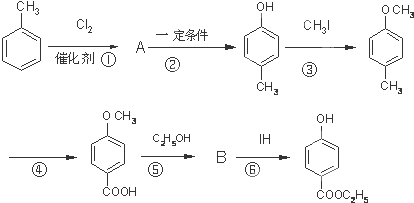
 .
. +CH3I→
+CH3I→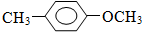 +HI
+HI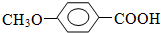 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$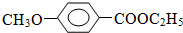 C2H5OH+H2O
C2H5OH+H2O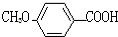 的同分异构体有多种,其中既含有酚羟基,又含有醇羟基和醛基的同分异构体共有13种,写出其中一种结构简式
的同分异构体有多种,其中既含有酚羟基,又含有醇羟基和醛基的同分异构体共有13种,写出其中一种结构简式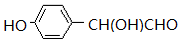 .
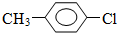
. 分析 甲苯和氯气反应生成A,A反应生成对甲基苯酚,由于A反应后得到的是对位取代的羟基,所以A的结构为对位取代的氯原子,故A为 ,③为取代反应、④为氧化反应,由
,③为取代反应、④为氧化反应,由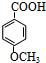 与乙醇发生反应生成B,B再HI作用下生成
与乙醇发生反应生成B,B再HI作用下生成 ,故B为
,故B为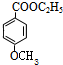 ;⑥为取代反应,再结合题目分析解答.
;⑥为取代反应,再结合题目分析解答.
解答 解:甲苯和氯气反应生成A,A反应生成对甲基苯酚,由于A反应后得到的是对位取代的羟基,所以A的结构为对位取代的氯原子,故A为 ,③为取代反应、④为氧化反应,
,③为取代反应、④为氧化反应,
由 与乙醇发生反应生成B,B再HI作用下生成
与乙醇发生反应生成B,B再HI作用下生成 ,故B为
,故B为 ;⑥为取代反应,
;⑥为取代反应,
(1)通过以上分析知,A结构简式为 ,故答案为:
,故答案为: ;
;
(2)反应③的化学方程式 +CH3I→
+CH3I→ +HI,
+HI,
故答案为: +CH3I→
+CH3I→ +HI;
+HI;
(3)反应⑤的化学方程式 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ C2H5OH+H2O,
C2H5OH+H2O,
故答案为: $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ C2H5OH+H2O;
C2H5OH+H2O;
(4)在合成路线中,反应③将羟基生成醚键,反应④用强氧化剂将甲基氧化成羧基,反应⑥将醚键生成酚羟基,酚羟基容易被氧化,所以设计③和⑥的目的是保护酚羟基不被氧化,
故答案为:保护酚羟基不被氧化;
(6)有机物 的同分异构体含有酚羟基、醇羟基和醛基,如果取代基为-OH、-CH(OH)CHO,有邻间对3种结构;
的同分异构体含有酚羟基、醇羟基和醛基,如果取代基为-OH、-CH(OH)CHO,有邻间对3种结构;
如果取代基为-OH、-CHO、-CH2OH,
如果-OH、-CHO相邻,有4种结构;
如果-OH和--CHO相间,有4种结构;
如果-OH、-CHO相对,有2种结构,
所以符合条件的有13种,其中一种结构简式为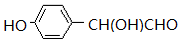 ,
,
故答案为:13;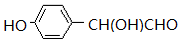 .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识综合运用能力,根据流程图中反应前后有机物结构变化确定反应类型及推断物质,难点是(6)题同分异构体种类判断,要考虑位置异构.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
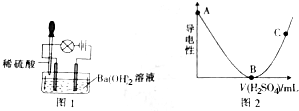
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{n(A-N+8)}{A+16}$ | B. | $\frac{n(A-N+10)}{(A+16)}$ | C. | A-N+2 | D. | $\frac{n(A-N+6)}{A}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2878KJ/mol | B. | 2658KJ/mol | C. | 1746KJ/mol | D. | 1526KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com