
分析 蛋白质具有盐析、变性等性质,其中在钠盐、铵盐、钾盐等溶液中发生盐析,为可逆过程,蛋白质没有失去生理活性,蛋白质在重金属盐溶液中可发生变性,失去生理活性,以此解答该题.
解答 解:向鸡蛋清中加入饱和硫酸铵溶液,可以观察到的现象为析出沉淀,说明饱和硫酸铵溶液可使蛋白质的溶解性变小,此过程叫做蛋白质的“盐析”为物理变化;再向试管里加入足量的蒸馏水,观察到的现象是变澄清,盐析是可逆过程,可以采用多次盐析的方法分离、提纯蛋白质,该过程中蛋白质没有失去生理活性,
故答案为:产生白色沉淀;盐析;沉淀溶解;可逆;没有.
点评 本题考查有机物的结构和性质,侧重考查蛋白质盐析的性质,为高频考点,题目难度不大,平时学习中注意蛋白质盐析和变性的在发生条件上、可逆性等方面的对比.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,6.72LO2和N2的混合气体含有的原子数为0.6NA | |
| B. | 通常状况下,8g O2和O3 的混合气体含有的分子数是0.5NA | |
| C. | 常温常压下,2mol/L的100mL MgCl2溶液中,含有Cl- 个数为0.4NA | |
| D. | 标准状况下,11.2L H2在氧气中完全燃烧后得到的产物的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 在反应中所有元素的化合价都发生变化 | |
| C. | 任何一个置换反应一定属于氧化还原反应 | |
| D. | 没有单质参与的化合反应和没有单质生成的分解反应不可能是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ②③⑤ | C. | ②③④ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
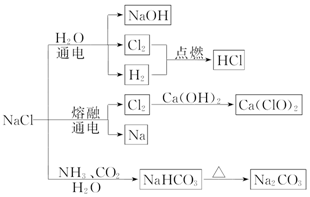
| A. | 25℃时,NaHCO3在水中的溶解度比 Na2CO3的大 | |
| B. | 石灰乳与 Cl2 的反应中,Cl2 既是氧化剂,又是还原剂 | |
| C. | 常温下干燥的 Cl2 能用钢瓶贮运,所以 Cl2 不与铁反应 | |
| D. | 图示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验目的 | 实验方法 |
| 证明地瓜粉中有淀粉 | B |
| 检验酒精中是否含有水 | C |
| 证明NaOH溶液呈碱性 | D |
| 除去FeCl2溶液中少量的FeCl3 | A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法.
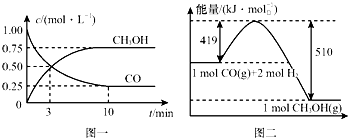
我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法.| 容器 | 反应物 投入的量 | 反应物的 转化率 | CH3OH 的浓度 | 能量变化(Q1、 Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1 kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2 kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温及加入催化剂都能使合成氨的反应速率加快 | |
| B. | H2、I2、HI平衡时的混合气体加压后颜色变深 | |
| C. | SO2催化氧化生成SO3的反应,往往需要使用催化剂 | |
| D. | 红棕色的NO2加压后颜色先变深后变浅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com