
| 卤素 | 氰 | 硫氰 | ① | |
| “单质” | X2 | (CN)2 | (SCN)2 | (OCN)2 |
| 酸 | HX | HCN | ② | HOCN |
| 盐 | KX | KCN | KSCN | ③ |
分析 (1)根据元素组成和物质的分类结合表中信息判断;
(2)①HSCN与二氧化锰共热反应类似于浓盐酸和二氧化锰共热反应;
②根据氯气和KOH反应书写(CN)2和KOH溶液反应方程式;
③因阴离子还原性强弱顺序为:Br-<CN-<SCN-<I-.所以在NaBr和KSCN溶液中加入少量(CN)2时,(CN)2只与SCN-反应.
解答 解:(1)从(CN)2和(SCN)2类推即可得出(OCN)2和(SCN)2的名称区别是元素S和O的区别,①应为氧氰,②应为HSCN,③为KOCN,
故答案为:氧氰;HSCN;KOCN;
(2)①HSCN与二氧化锰共热反应类似于浓盐酸和二氧化锰共热反应,所以该离子反应方程式为4H++2SCN-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++(SCN)2↑+2H2O,
故答案为:4H++2SCN-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++(SCN)2↑+2H2O;
②(CN)2和KOH溶液反应类似氯气和氢氧化钾的反应:Cl2+2KOH=KCl+KClO+H2O,则(CN)2和KOH溶液反应的化学方程式为(CN)2+2KOH=KCN+KOCN+H2O,
故答案为:(CN)2+2KOH=KCN+KOCN+H2O;
③由还原能力的大小信息可知:(CN)2只能氧化SCN-而不能氧化Br-,在NaBr和KSCN的混合溶液中加入(CN)2只发生(CN)2+2SCN-=2CN-+(SCN)2,
故答案为:(CN)2+2SCN-=2CN-+(SCN)2.
点评 本题考查卤族元素性质递变规律,为高频考点,侧重考查学生知识迁移能力,根据卤素单质性质采用知识迁移方法来分析解答即可,关键是找出物质之间的相似性,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L甲醇中含有的原子总数为0.6NA | |
| B. | 室温下,500mL pH=1的稀硫酸中含有的H+总数约为0.05NA | |
| C. | 7.8g Na2O2晶体中含有的离子总数为0.4NA | |
| D. | 电解精炼铜时,若阴极得到电子总数为2NA,则阳极质量减少64g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A,B用导线连接后浸入电解质溶液,结果电子从B流向A | |
| B. | A从酸中置换出H2比B从酸中置换H2难 | |
| C. | 1 mol A从酸中置换出H十生成的H2比1mol B从酸中置换出H十生成的H2多 | |
| D. | 常温时,A能从水中置换出氢气,而B不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯分子里所有的原子在同一平面上 | |
| B. | 乙烯的结构简式为CH2CH2,电子式为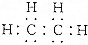 | |
| C. | 乙烯分子中碳氢键之间的夹角约为120° | |
| D. | 乙烯分子中既含有极性键又含有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
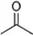 根据键线式回答下列问题:
根据键线式回答下列问题: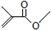 分子式:C5H8O2,
分子式:C5H8O2,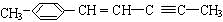 分子中最多有4个原子共直线;
分子中最多有4个原子共直线;
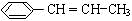 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式: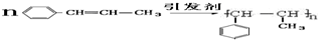 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
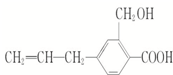 某有机物的结构简式为如右图所示,其可能具有的性质是( )
某有机物的结构简式为如右图所示,其可能具有的性质是( ) | A. | 全部 | B. | 仅能发生①②③④ | C. | 除⑤外都能 | D. | 除④⑤外都能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 molAl3+含有的核外电子数为3NA | |
| B. | 将58.5g NaCl溶于1.00 L水中,所得NaCL溶液的浓度为1.00mol•L-1 | |
| C. | 1 molCl2与足量的铁反应,转移的电子为数3Na | |
| D. | 常温下,10LpH=1的硫酸溶液中含有的H+离子数为NA. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 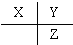 | B. | 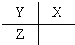 | C. | 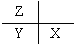 | D. | 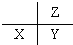 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com