
| A、过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 |
| B、NH4HCO3溶液中加入过量的NaOH溶液并加热:HCO3-+OH-═CO32-+H2O |
| C、稀硝酸除银镜:Ag+2H++NO3-═Ag++NO↑+H2O |
| D、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═Fe2++I2 |
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
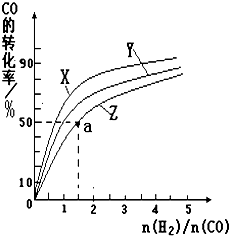 甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:| 1 |
| 2 |
| 1 |
| 2 |
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中加入Ba(NO3)2溶液后产生白色沉淀,则原溶液中一定含有SO42- |
| B、向某稀溶液中加入Ba(NO3)2溶液后无明显现象,再滴入几滴硝酸酸化的AgNO3溶液,产生白色沉淀,说明一定是氯化物的溶液 |
| C、将盛满H2的小试管管口向上靠近酒精灯火焰检验H2的纯度 |
| D、将燃着的木条靠近导管口,木条熄灭,说明有CO2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从海水中提取氯化钠的过程涉及化学反应 |
| B、从海带中提取碘单质的过程涉及置换反应 |
| C、从海水中提取溴单质的过程涉及氧化还原反应 |
| D、海水中含有氯化钠等多种氯化物;除了氯,海水中溴的储量也很高,溴也被称为“海洋元素” |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、NaCl是非电解质 |
| B、NaCl溶液是电解质 |
| C、NaCl在水溶液中电离出了可以自由移动的离子 |
| D、NaCl溶液中产生了电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com