
(1)14.2gC12含_________个氯气分子,_______摩尔氯原子,标准状况下所占的体积为________升,与这些Cl2分子数相同H2的质量是__________g,它们恰好完全反应后得到的氯化氢气体的物质的量是________摩尔,质量为________g,在标准状况下是_______升,将产生的氯化氢气体溶于490.4 mL水中,则所得溶液的质量为________g,若所得溶液的密度为1.01g/cm3,则该溶液的体积为_________ L。溶液的物质的量浓度为_________mol/L,质量分数为__________。
(2)在下列物质:① 烧碱②SO3 ③ 铁片④ 石墨⑤ 甲烷 ⑥醋酸 ⑦盐酸 ⑧硫酸钡,属于电解质的是__________(请填序号,下同),其中属于强电解质的是____________,属于非电解质的是__________,既不属于电解质又不属于非电解质的是____________。
(3)标准状况下,1 体积水能溶解448 体积HCl,所得溶液的密度为1.2g/mL,该溶液的质量分数和物质的量的浓度分别是____________、_____________。(保留1位小数)
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:2016-2017学年黑龙江省哈尔滨市四校高一期中联考化学试卷(解析版) 题型:计算题
(要求有 计算过程)
计算过程)
用KMnO4氧化一定体积密度为1.19g/cm3,溶质质量分数为36.5%的盐酸。
反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法分析该反应(只需标出电子得失的方向和数目)
(2)15.8g KMnO4参加反应能消耗多少摩尔HCl?
(3)产生的Cl2在标准状况下的体积为多少升?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高一上学期期中化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.常温常压下,48 g O3中的氧原子数为3NA
B.24 g金属镁变为镁离子时失去的电子数为NA
C.4℃时9 mL水和标准状况下11.2 L氮气中的原子数均为NA
D.2 mol.L-l的CuCl2溶液中含有的氯离子数为4NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高二上学期期中化学试卷(解析版) 题型:选择题
能说明反应N2+3H2 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
A.1个N≡N键断裂的同时,有3个H-H键形成
B.1个N≡N键断裂的同时,有3个H-H键断裂
C.1个N≡N键断裂的同时,有2个N-H键断裂
D.1个N≡N键断裂的同时,有6个N-H键形成
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:计算题
工业电解饱和食盐水产生的氯气制漂白粉,所进行的反应是
① 2NaCl+2H2O Cl2+H2+2NaOH
Cl2+H2+2NaOH
② 2Ca(OH)2(石灰乳)+ 2Cl2 =CaCl2+Ca(ClO)2+2H2O
某厂日产漂白粉(含量80%,主要杂质Ca(OH)2)20吨,已知进行①步反应的转化率90%,进行②步转化率85%。
(1)写出②反应的离子方程式并用双线桥标出电子转移数目
(2)列式计算该厂日消耗精制后的NaCl多少摩尔?(科学计数值,保留小数点后两位)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
实验室中需用2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是
A.950mL 111.2g B.500mL 117.0g
C.1000mL 117.0g D.1000mL 111.2g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
下列物质中,不会出现丁达尔效应的分散系是( )
①氢氧化铁胶体②水③豆浆④蔗糖溶液⑤FeCl3溶液⑥云、雾
A.②④⑤ B.③④ C.②④⑥ D.④①③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上期中化学卷(解析版) 题型:填空题
芦笋中的天冬酰胺(结构如右图)和微量元素硒、铬锰等,具有提高身体免疫力的功效。
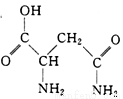
(1)天冬酰胺所含元素中, (填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有 种。
(3)H2S和H2Se的参数对比见下表。
化学式 | 键长/nm | 键角 | 沸点/℃ |
H2S | 1.34 | 92.3º | -60.75 |
H2Se | 1.47 | 91.0º | -41.50 |
①H2Se的晶体类型为 ,含有的共价键类型为 。
②H2S的键角大于H2Se的原因可能为 。
(4)已知铝(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示
编号 | I5/KJ·mol-1 | I6/KJ·mol-1 | I7/KJ·mol-1 | I8/KJ·mol-1 |
A | 6990 | 9220 | 11500 | 18770 |
B | 6702 | 8745 | 15455 | 17820 |
C | 5257 | 6641 | 12125 | 13860 |
A是 (填元素符号),B的价电子排布式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高二上学期期中化学试卷(解析版) 题型:选择题
已知分解1mol KClO3放出热量38.8kJ,在MnO2下加热,KClO3的分解机理为:
①2KClO3+4MnO2 2KCl+2Mn2O7 慢
2KCl+2Mn2O7 慢
②2Mn2O7 4MnO2+3O2 快
4MnO2+3O2 快
下列有关说法不正确的是( )
A.1 mol KClO3所具有的总能量高于1 mol KCl所具有的总能量
B.KClO3分解速率快慢主要取决于反应①
C.1 g KClO3 ,1 g MnO2,0.1 g Mn2O7混合加热,充分反应后MnO2质量为1 g
D.将固体二氧化锰碾碎,可加快KClO3的分解速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com