
����Ŀ��I��KI����������Һ�м������������Һ��Ѹ�ٷ�Ӧ�ų��������ݣ���Һ����ɫ��
��������֪����Ӧ�������£�
��H2O2+2KI+H2SO4=I2+K2SO4+2H2O��
��H2O2+I2=2HIO�� ��H2O2+2HIO=I2+O2��+2H2O
��1����˫���ŷ���ʾ���̢ٵ���ת�������H2O2+2KI+H2SO4=I2+K2SO4+2H2O
��2������ʵ����̢�����У�I2���������ã�
��3�����жϣ�����������HIO��H2O2��O2�������������Ե�ǿ�������ѧʽ����
���𰸡�
��1��
��2������
��3��H2O2��HIO��O2
���������⣺��1��H2O2+2KI+H2SO4=I2+K2SO4+2H2O��O�ө�1�۽��͵���2�ۣ�I�ө�1�����ߵ�0�ۣ�ת�Ƶ�����Ϊ2������˫���ŷ���ʾ����ת��Ϊ 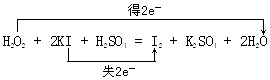 ��
��
��2����Ӧ�����У�I2���뷴Ӧ�����������ɵ�����I2���ӿ��������ķֽ⣬I2��������ã�
��3���ɢ�H2O2+I2��2HIO����֪�����ԣ�H2O2��HIO���ɢ�H2O2+2HIO��I2+O2��+2H2O����֪�����ԣ�HIO��O2���������ԣ�H2O2��HIO��O2��
�ʴ�Ϊ����1�� ����2����������3��H2O2��HIO��O2
����2����������3��H2O2��HIO��O2
��1����˫���ű�ʾ����ת��ʱ��Ӧע���ͷָ�����ͬһ��Ԫ�أ�
��2�������ڻ�ѧ��Ӧǰ���������ͻ�ѧ���ʱ��ֲ��䣻
��3�����ݡ��������������Դ�����������������ԡ����з���ȷ����


 �ľ�ͼ���ʱ�ȷ�ϵ�д�
�ľ�ͼ���ʱ�ȷ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Wԭ�ӵ����������������ڲ��������3���������ж���ȷ���ǣ� �� 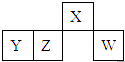
A.ԭ�Ӱ뾶��W��Z��Y��X
B.��YԪ�ص�����Һһ��������
C.�����̬�⻯������ȶ��ԣ�Z��W
D.X����Ԫ����ɵĻ�����XH5��ˮ��Ӧ�ɲ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л������У���ֻ����һ�ֻ��������(����)
A. CH4B. C2H6C. C3H8D. C4H10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ƵĻ�ѧ���ʺͻ�ѧ��Ӧ�����෨�����ü�����������ģ�
��1����������5�����ʣ�CuO��CO��MgO��Na2O��FeO�����ղ�ͬ�ķ��������������1������������4�����������ԵIJ�ͬ���ҳ��������ʣ���д�����ݣ�д�����֣���
����
�� ��
��2����Ȼ����ķ�����ͬ�������ӷ�Ӧ��������ԭ��Ӧ֮��Ҳ������һ���Ĺ�ϵ���ü�ͼʾ������ʾ����֮��Ĺ�ϵ ��
��3�������е�ʳ�Ͷ����ֱ����ڷ�ɢϵ�е��� �� �����Լ����ѧר�����ʣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԭ��ص��ܷ�Ӧ�����ӷ���ʽ��Zn + Cu2+ �� Zn2+ + Cu����ԭ��ص������ȷ���ǣ�
���� | ���� | �������Һ | |
A | Zn | Cu | CuCl2 |
B | Ag | Cu | H2SO4 |
C | Cu | Zn | CuSO4 |
D | Cu | Zn | FeCl2 |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ƭ��̼����ͼ��ʾ��ʽ��������ͭ��Һ�У�������ָ�뷢��ƫת��������Ը�װ�D��˵������ȷ���ǣ�������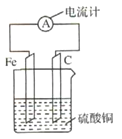
A.̼��������
B.��װ���ܽ�����ת��Ϊ��ѧ��
C.���·�е�������Ƭ������������������̼��
D.��װ�õ��ܷ�ӦΪ��2Fe+3Cu2+=2Fe3++3Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����������������������ȡ������ú�����Fe2+��Fe3+������������Һ�����ȵ�һ���¶ȣ����裬����һ�������������Һ����������Һ������Һ�����ɻ��Զ������̣�������Һ��pH����Ӧһ��ʱ�䣬Fe��OH�� 3�Ͷ������̷��������������ã����յõ��������������壮 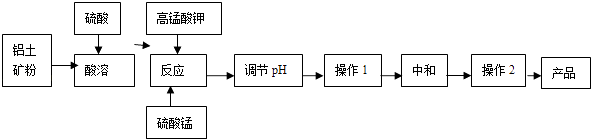
��1��KMnO4���Ƚ�Fe2+����ΪFe3+ �� �䱾������ԭΪMnO2 �� ��Ӧ�����ӷ���ʽΪ ��
��2��д�����������Һ����������Һ��Ӧ�Ļ�ѧ����ʽ �� ʵ��֤����n��MnO2��/n��Fe��������4��1ʱ������Ч���Ϻã�����Һ���������Ӻ�������Ũ�Ⱦ�Ϊ0.03mol/L��Ϊ�ﵽ�Ϻõij���Ч����ÿ1L��ҺӦ���������ص����ʵ���Ϊ ��
��3������pH�������� ��
��4������1������Ϊ �� ����2������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1mol NO��1mol NO2������ͬ��:�ٷ���������ԭ�������۵�ԭ����������ԭ������
A. �٢� B. �ڢ� C. �٢� D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O������������ȷ���ǣ�������
5NaCl+NaClO3+3H2O������������ȷ���ǣ�������
A.Cl2����������NaOH�ǻ�ԭ��
B.����������ԭ�Ӻͱ���ԭ����ԭ�ӵ����ʵ���֮��Ϊ5��1
C.Cl2����������������ԭ��
D.�������õ������뻹ԭ��ʧ������֮��Ϊ5��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com