
【题目】下列离子方程式书写不正确的是
A. 碳酸钙和稀盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
B. 钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+
C. 将金属铝加入NaOH溶液中:2Al+2OH+2H2O=2AlO2+3H2↑
D. 金属钠与水反应:2Na+2H2O=2Na++2OH+H2↑
【答案】B
【解析】
A.二者反应生成氯化钙、水和二氧化碳;B.钠先与水反应,生成的氢氧化钠再与硫酸铜反应;C.铝与氢氧化钠溶液反应生成偏铝酸钠与氢气;D.金属钠与水反应生成氢氧化钠和氢气。
A.碳酸钙和稀盐酸反应,离子方程式: CaCO3+2H+===Ca2++CO2↑+H2O,A正确;B.钠先与水反应生成氢氧化钠和氢气,然后氢氧化钠与硫酸铜反应生成氢氧化铜蓝色沉淀,不能置换出铜,故B错误;C.铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为: 2Al+2OH-+2H2O===2AlO![]() +3H2↑,C正确;D.金属钠与水反应生成氢氧化钠和氢气,离子方程式为: 2Na+2H2O===2Na++2OH-+H2↑,D正确;正确选项B。
+3H2↑,C正确;D.金属钠与水反应生成氢氧化钠和氢气,离子方程式为: 2Na+2H2O===2Na++2OH-+H2↑,D正确;正确选项B。


科目:高中化学 来源: 题型:
【题目】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备,正丁烷(C4H10)催化脱氢制1-丁烯(C4H8) 的化学方程式如下:C4H10(g)=C4H8(g)+H2(g)△H,如图是该反应平衡转化率与反应温度及压强的关系图,下列说法正确的是
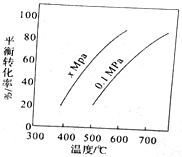
A. x>0.1
B. △H>O
C. 500C时,压强xMPa比0.1MPa条件下的平衡常数大
D. 一定温度下,在一恒容密闭容器中发生该反应,C4H10的浓度越高,平衡转化率越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是__________________________________________________。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)______________________________。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2 mol·L-1, c(Fe3+)=1.0×10-3 mol·L-1,c(Cl-)=5.3×10-2 mol·L-1,则该溶液的pH约为________。
②完成NaClO3氧化FeCl2的离子方程式:
![]() ClO3-+
ClO3-+![]() Fe2++________===
Fe2++________===![]() Cl-+
Cl-+![]() Fe3++
Fe3++![]() ________,______________
________,______________
(3)FeCl3在溶液中分三步水解:
Fe3++H2O ![]() Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O![]() Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++H2O![]() Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是________________。
通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为xFe3++yH2O![]() Fex(OH)
Fex(OH)![]() +yH+,欲使平衡正向移动可采用的方法是(填序号)________。
+yH+,欲使平衡正向移动可采用的方法是(填序号)________。
a.降温 b.加水稀释
c.加入NH4Cl d.加入NaHCO3
(4)天津某污水处理厂用聚合氯化铁净化污水的结果如图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为________mg·L-1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。

(1)B装置中的干燥剂是_____(填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是_____(填”C”或“D”)。
(3)当实验进行段时间后,挤压E装置中的胶头滴管,滴入1--2滴浓盐酸,可观察到E装置中的现象是产生______(填”烟”或“白雾”)。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_____(填“F”或“G”)。
(5)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是____(填“a”“b”或“c”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.钠保存在煤油中
B.氯水保存在棕色试剂瓶中
C.Na2O2需要隔绝空气密封保存
D.实验室盛装NaOH溶液的试剂瓶用玻璃塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液组成的描述合理的是( )
A. 无色强碱性溶液中可能大量存在Al3+、N![]() 、Cl-、S2-
、Cl-、S2-
B. 酸性溶液中可能大量存在Na+、ClO-、HC![]() 、I-
、I-
C. 弱碱性溶液中可能大量存在Na+、K+、Cl-、S![]()
D. 无色中性溶液中可能大量存在Fe3+、K+、Cl-、S![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从氧化还原角度分析,下列反应中水的作用相同的是
① 铁和水蒸气反应 ② 过氧化钠和水反应
③氯气和水反应 ④ 二氧化氮和水反应3NO2+H2O=2HNO3+NO
A.①②③B.①②④C.②③④D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子数总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8;E与B的质量比为1:1。试回答:
(1)写出基态D原子的电子排布式_______________________。
(2)用电子式表示AE2的形成过程_______________,与AE2互为等电子体的离子是_______。
(3)相同条件下EB2分子和AB2分子两者在水中的溶解度较大的是____(写分子式),理由是
______________________________。
(4)根据VSEPR模型预测C的氢化物的立体结构为_________,B、C两元素的气态氢化物的稳定性大小关系为:_____________(填写化学式)。
(5)C的单质中π键的数目为___,晶体D的晶胞中的所含原子数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
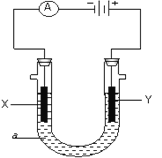
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则可观察到在X极附近观察到的现象是__________电极反应式是________________检验Y电极反应产物的方法是____________________电解一段时间之后溶液的PH将会________(升高、降低或不变),总方程式为_________________________。
(2)若X、Y都是铜电极,a是稀CuSO4溶液,开始实验,X极的电极反应式是__________________________。电解前后CuSO4溶液的浓度___________________(变大、变小或不变)若X电极质量增重64克,则在电路中有_________________mol的电子发生转移。
(3)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则①X电极的材料是_____,电极反应式是_____________。②Y电极的材料是______,电极反应式是____________________。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com