
【题目】下列事实不能用勒夏特列原理解释的是
A.溴水中存在Br2+H2O![]() HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
B.反应CO(g)+NO2(g) ![]() CO2(g)+NO(g) ΔH<0,平衡后,升高温度体系颜色变深
CO2(g)+NO(g) ΔH<0,平衡后,升高温度体系颜色变深
C.用饱和食盐水除去Cl2中的HCl
D.合成氨反应,为提高氨的产率,可加入适当的催化剂
【答案】D
【解析】
勒夏特列原理:当影响平衡移动的因素改变后,平衡会向减弱这种条件的方向移动。据此回答本题。
A、当加入硝酸银溶液后,硝酸银与溴化氢反应产出溴化银沉淀,溴化氢减少,使可逆反应正向移动,溶液颜色变浅,故A正确;
B、升高温度,平衡向吸热反应方向移动,即逆向移动,NO2的含量增加,颜色变深,故B正确;
C、Cl2与水的离子反应方程式为:Cl2+H2O![]() H++Cl-+HClO,饱和食盐水中含有大量的Cl-,使反应逆向移动,降低Cl2的溶解度,HCl在水中溶解度很大,所以能用饱和食盐水除去Cl2中的HCl,故C正确;
H++Cl-+HClO,饱和食盐水中含有大量的Cl-,使反应逆向移动,降低Cl2的溶解度,HCl在水中溶解度很大,所以能用饱和食盐水除去Cl2中的HCl,故C正确;
D、催化剂只改变化学反应速率,不影响平衡移动,故D错误;
故选D。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】化学与人类的生活、生产息息相关,下列说法正确的是
A.氯水和食盐水消毒杀菌的原理相同
B.制造普通玻璃的原料为石英砂、石灰石和纯碱
C.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D.可以用钢瓶储存液氯和浓H2SO4,因为它们对钢瓶发生了钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际贸易可以互通有无,符合国际社会的根本利益,下列贸易商品中,主要成分属于无机物的是
A.巴西铁矿砂 | B.沙特石油 | C.俄罗斯天然气 | D.中国丝绸 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu发生的氧化还原反应,实验记录如下表所示,下列说法错误的是( )
序号 | Ⅰ | Ⅱ | Ⅲ |
实验步骤 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜有剩余,溶液黄色褪去,变成蓝色加入蒸馏水后无白色沉淀 |
A.实验Ⅰ、Ⅱ、Ⅲ中均涉及Fe3+被还原
B.对比实验Ⅰ、Ⅱ、Ⅲ说明白色沉淀的产生可能与铜粉的量及溶液中阴离子种类有关
C.实验Ⅱ、Ⅲ中加水后c(Cu2+)相同
D.向实验Ⅲ反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组在探究淡黄色过氧化钠与水反应是放出热量还是吸收热量时设计了如图所示的实验装置。

在小试管里加入1g淡黄色过氧化钠,把小试管套在带支管的试管内。在U形管内加入少量红墨水。打开T形管螺旋夹,使U形管内两边的液面处于同一水平面。再夹紧螺旋夹,把水滴入小试管内,可观察到U形管右侧的液面立即下降,左侧的液面上升。
(1)过氧化钠的电子式__。
(2)写出上述反应的化学方程式__。
(3)下列各图中,表示过氧化钠与水反应的图是(_______)
A.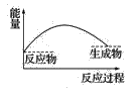 B.
B.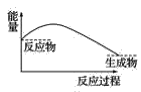
C.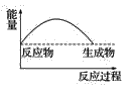 D.
D.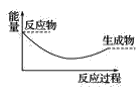
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项比较中,一定相等的是
A.相同质量的 Fe 完全转化为FeCl2和FeCl3 时转移的电子数
B.相同质量的苯和乙炔所含的碳原子的数目
C.标准状况下的 2.24 L HCl 气体和1 L 0.1 mol·L1盐酸中所含Cl的数目
D.相同物质的量浓度的NH4Cl和(NH4)2Fe(SO4)2溶液中 NH![]() 的浓度
的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱金属都能与氧气反应:
(1)已知1.4 g锂在空气中加热充分反应,可生成3.0 g氧化物,写出该反应的化学方程式: ______。
(2)将一小块金属钠、钾分别投入到加热的坩埚中,观察到的实验现象是____________,有关反应的化学方程式是______________。
(3)由上述实验得出的结论是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种锂离子电池的反应式为 LixC6 + Li1xCoO2![]() 6C+LiCoO2(x<1)。其工作原理如图所示。下列说法不正确的是
6C+LiCoO2(x<1)。其工作原理如图所示。下列说法不正确的是
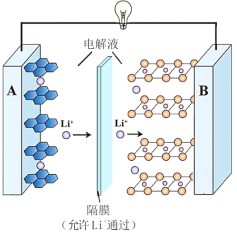
A.放电时,A 极电极式为:LixC6 xe = 6C + xLi+
B.放电时,若转移 0.3 mol 电子,石墨电极将减重 2.1g
C.充电时,Li+从左向右移动
D.若要从废旧该型锂电池的正极材料中回收锂元素,先进行放电处理,有利于 Li+尽可能从负极脱出,在正极富集
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4超干重整CO2技术可得到富含CO的化工原料。回答下列问题:
(1)CH4超干重整CO2的催化转化如图所示:
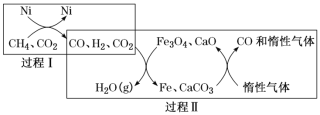
①已知:CH4(g)+H2O(g)=CO(g)+3H2(g) △H1=+206.2kJ/mol ;
CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H2=-165kJ/mol;
过程I的热化学方程式为_______。
②关于上述过程II的说法不正确的是______(填字母)。
a.实现了含碳物质与含氢物质的分离 b.可表示为CO2+H2H2O(g)+CO c.CO未参与反应 d.Fe3O4、CaO为催化剂,降低了反应的ΔH
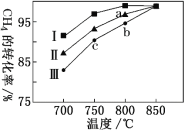
③其他条件不变,在不同催化剂(I、II、III)作用下,反应CH4(g)+CO2(g) 2CO(g)+2H2(g)进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点是否达到平衡状态?________(填“是”或“否”);b点CH4的转化率高于c点,原因是________。
(2)在刚性密闭容器中,加入CH4和CO2,二者分压分别为20 kPa、25 kPa,加入Ni/α-Al2O3催化剂并加热至1123 K使其发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g)。
①研究表明CO的生成速率v(CO)=1.3×10-2·p(CH4) ·p(CO2)。(单位忽略),某时刻测得p(CO)=20 kPa,则p(CO2)=________kPa,v(CO)=________(单位忽略)。
②达到平衡后测得体系压强是起始时的1.8倍,则该反应的平衡常数的计算式为Kp=________。(用各物质的分压计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com