
 ),其原理如图1所示.
),其原理如图1所示.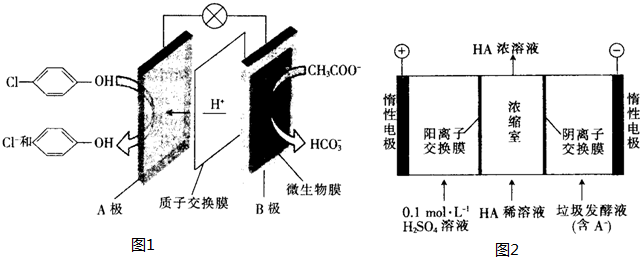
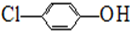
 -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-.
-OH+Cl-.分析 (1)①根据原电池中阳离子的移动方向确定正负极;
②根据原电池中正极上得电子结合正极反应物来分析解答;
(2)①电解池中阳极上氢氧根离子失电子生成氧气;
②根据电解池中离子移动方向来回答判断.
解答 解:(1)①原电池中氢离子的移动方向是从负极流向正极,所以B是电池的负极,故答案为:负;
②A是正极,正极上发生得电子的还原反应:Cl- -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-,故答案为:Cl-
-OH+Cl-,故答案为:Cl- -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-;
-OH+Cl-;
(2)①阳极上是阴离子氢氧根离子发生失电子的氧化反应,电极反应式为:4OH--4e-═2H2O+O2↑,故答案为:4OH--4e-═2H2O+O2↑;
②在电解池的阳极上是OH-放电,所以c(H+)增大,并且H+从阳极通过阳离子交换膜进入浓缩室;根据电解原理,电解池中的阴离子移向阳极,即A-通过阴离子交换膜从阴极进入浓缩室,这样:H++A-═HA,乳酸浓度增大,
故答案为:阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室,A-通过阴离子交换膜从阴极进入浓缩室,H++A-═HA,乳酸浓度增大.
点评 本题涉及电解池和原电池的工作原理以及应用的考查,注意知识的迁移和应用是解题的关键,难度中等,注意把握原电池和电解池中离子的移动方向.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:解答题
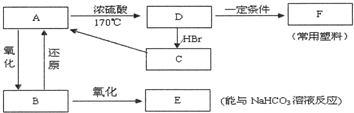
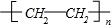
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用蓝绿藻等低等植物和微生物在阳光作用下使水分解产生氢气,该方法符合绿色化学原则 | |
| B. | 12C、13C和14C互为同位素,它们的放射性可用于考古断代,可测定生物体死亡的年代 | |
| C. | 超高分辨荧光显微镜可以观察到纳米世界,其中利用了荧光蛋白,生物发光也与荧光蛋白有关,生物发光是将化学能转化为光能的过程 | |
| D. | 分子筛中有许多笼状空穴和通道可用于分离、提纯气体,还可用作干燥剂、离子交换剂、催化剂和催化剂载体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液:Na+、Fe3+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | |
| B. | 滴入甲基橙呈红色的溶液中:K+、HCO${\;}_{3}^{-}$、Cl-、CO${\;}_{3}^{2-}$ | |
| C. | c(OH-)=1.0×10-13mol•L-1的溶液中:SO${\;}_{3}^{2-}$、SiO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$、K+ | |
| D. | c(I-)=0.1 mol•L-1的溶液中:Na+、NH${\;}_{4}^{+}$、ClO-、SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用H2作为燃料的优点之一是燃烧后的产物不污染环境 | |
| B. | 要使海水淡化通常有蒸馏法和离子交换法 | |
| C. | 冶炼金属铝通常用电解氯化铝的方法 | |
| D. | 煤的干馏属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 “盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O=2Mg(OH)2.下列关于该电池的说法错误的是( )
“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O=2Mg(OH)2.下列关于该电池的说法错误的是( )| A. | 镁片作为正极 | |
| B. | 食盐水作为电解质溶液 | |
| C. | 电池工作时镁片逐渐被消耗 | |
| D. | 电池工作时实现了化学能向电能的转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com