
【题目】下列物质中,能够导电的电解质是
A. Cu B. 熔融的MgCl2 C. 氢氧化钠溶液 D. 蔗糖
科目:高中化学 来源: 题型:
【题目】阅读相关信息,结合所学知识,回答下列问题:
(1)铝和锌都是两性金属元素。其氢氧化物都是白色沉淀,既能溶于强酸,又能溶于强碱(生成AlO2-或ZnO22-)。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。
①写出锌和氢氧化钠溶液反应的化学方程式_________________________________。
②用氨水除去Al(OH)3中的Zn(OH)2的离子方程式为__________________________。
③写出向AlCl3溶液中滴入过量氨水的离子方程式___________________________;
向ZnCl2溶液中逐滴滴入氨水直至过量的现象是___________________________。
④下列各组中的两种溶液,只用胶头滴管和试管即可鉴别的是________________。
A.硫酸铝和氢氧化钠 B.硫酸铝和氨水
C.硫酸锌和氢氧化钠 D.硫酸锌和氨水
(2)Cu2O是一种红色难溶于水的固体,在空气中灼烧Cu2O会生成CuO;Cu2O溶于稀硫酸可生成Cu和Cu2+;Cu2O和Cu都能溶于稀硝酸。
研究性学习小组为检测Cu样品中是否含有Cu2O设计以下实验方案:
方案Ⅰ:取该红色样品溶于足量的稀硝酸中,观察是否有残渣剩余
方案Ⅱ:取该红色样品溶于足量的稀硫酸中,观察溶液颜色变化
方案Ⅲ:称量a g红色样品,在空气中充分灼烧至恒重,得到bg黑色固体。
①比较方案Ⅰ和方案Ⅱ,你认为合理的是方案_________(填“Ⅰ”或“Ⅱ”),合理方案的反应原理为________________________________________(用离子方程式表示)。
②方案Ⅲ中,如果 < b < (用含a的代数式表示)____________,可确认红色粉末含有Cu2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氯化镁和氯化铝的200 mL 混合溶液中,c(Mg2+)为 0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为( )
A. 40 mL B. 72 mL C. 80 mL D. 128 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I甲、乙、丙、丁分别是由H+、Na+、Al3+、Ba2+、OH-、Cl-、HCO3- 离子中的两种组成,可以发生如图转化:
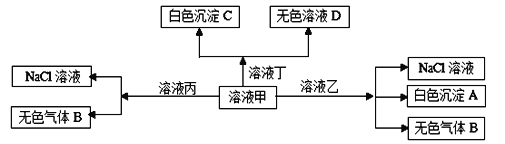
(1)写出无色气体B的一种用途_____________________________。
(2)甲与乙反应的离子方程式为:____________________________。
(3)白色沉淀A可能溶解在溶液D中,其溶解的化学方程式为:________________。
II无水NiCl2在有机合成中有着极为重要的作用,工业上常用含镍原料所制得的NiCl2·6H2O在亚硫酰氯(SOCl2)中加热脱水制得,已知SOCl2能与水反应生成SO2和HCl。写出NiCl2·6H2O在亚硫酰氯(SOCl2)中加热脱水制无水NiCl2的化学方程式___________________________________,NiCl2·6H2O需在亚硫酰氯(SOCl2)中加热脱水的原因是________________________________。
III锰及其化合物用途广泛。锰的化合物有60多种,其中以二氧化锰(MnO2)最稳定。将固体草酸锰(MnC2O4·2H2O)放在一个可以称出质量的容器里加热。固体质量随温度的变化关系如图所示,则:214 ℃时,剩余固体的成分为___________(填化学式); 943 ℃时,剩余固体的成分为__________(填名称)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 甲苯分子中所有原子在同一平面上
B. 苯、乙酸、乙醇均能发生取代反应
C. 分子式为C3H6Cl2的同分异构体共有4种(不考虑立体异构)
D. 可用溴的四氯化碳溶液区别![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤气中主要的含硫杂质有H2S以及COS(有机硫),煤气燃烧后含硫杂质会转化成SO2从而引起大气污染,因此煤气中H2S的脱出程度已成为煤气洁净度的一个重要指标。请回答下列问题:
(1)H2S在水溶液中的电离方程式为___________。
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法、水解法等。
①COS的分子结构与CO2相似,COS的结构式为___________。
②Br2的KOH溶液将COS氧化为硫酸盐的离子方程式为______________。
③已知:H2、COS、H2S、CO的燃烧热依次为285kJ/mol、299kJ/mol、586kJ/mol、283kJ/mol;H2还原COS发生的反应为H2(g)+COS(g)=H2S(g)+CO(g),该反应的ΔH=_________kJ/mol。
④用活性α-Al2O3催化COS水解反应为COS(g)+H2O(g) ![]() CO2(g)+H2S(g) ΔH<0,相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与n(H2O)/n(COS)的关系如图2所示。
CO2(g)+H2S(g) ΔH<0,相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与n(H2O)/n(COS)的关系如图2所示。
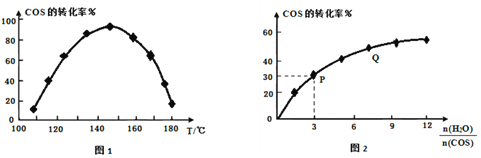
由图1可知,催化剂活性最大时对应的温度约为______,COS的转化率在后期下降的原因是_______________________________________。由图2可知,P点时平衡常数K=______(保留2位有效数字)。Q点转化率高于P点的原因是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,0.1mol/L某一元酸HA的水溶液PH=4.下列描述不正确的是( )
A.该溶液中HA有0.1%发生了电离
B.此酸电离平衡常数约为10﹣7
C.升高温度后溶液的PH增大
D.若将PH=2的HA溶液与PH=12的NaOH溶液等体积混合后PH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 液溴易挥发,在存放液溴的试剂瓶中应加水封
B. 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
C. 某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
D. 某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com