
【题目】酒石酸托特罗定用于治疗泌尿系统疾病。工业合成该药物中间体(F)的路线如下:

己知:
回答下列问题:
(1)D分子中的含氧官能团名称为_________、_______________;B→C包含两步反应,反应类型分别为_______、______________。
(2)A的结构简式为______________________。
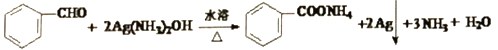
(3)写出苯甲醛与银氨溶液反应的化学方程式________________________________。
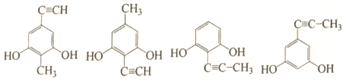
(4)B的一种同分异构体满足下列条件:①能使溴的CCl4溶液褪色;②能与FeCl3溶液发生显色反应;③分子中有4种不同化学环境的氢。写出该同分异构体的结构简式_______________。(任写一种)
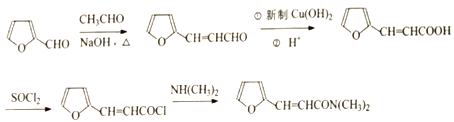
(5)已知呋喃丙胺(![]() CH=CHCON(CH3)2)是一种高效麻醉剂,写出以
CH=CHCON(CH3)2)是一种高效麻醉剂,写出以![]() 、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选)。合成路线流程图示例如下:_____________
、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选)。合成路线流程图示例如下:_____________
H2C=CH2![]() CHCH2Br
CHCH2Br![]() CH3CH2OH
CH3CH2OH
【答案】 羧基 醚键 加成 取代(酯化) ![]()
【解析】试题分析:(1)由D的结构简式可知,含有的含氧官能团为羧基、醚键;对比B、C结构可知,B与对甲基苯酚发生酯化反应,属于取代反应,甲基间位的C-H键断裂与碳碳双键发生加成反应形成六元环;
(2)由信息可知,对比苯甲醛与乙醛反应得到A为![]() ;
;
(3)苯甲醛与银氨溶液反应氧化反应得到苯甲酸铵、Ag、氨气与水,反应方程式为
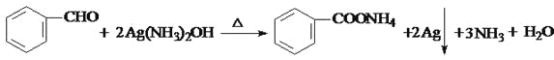 ;
;
(4)B的一种同分异构体满足下列条件:①能使溴的CCl4溶液褪色,说明含有不饱和键,可以是碳碳三键等,②能与FeCl3溶液发生显色反应,说明含有酚羟基,③分子中有4种不同化学环境的氢,符合条件的同分异构体有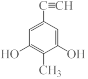
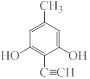
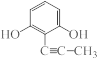
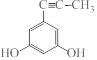 等;
等;
(5)![]() 与CH3CHO在氢氧化钠、加热条件下得到
与CH3CHO在氢氧化钠、加热条件下得到![]() ,再用新制氢氧化铜氧化、然后酸化得到
,再用新制氢氧化铜氧化、然后酸化得到![]() ,再与SOCl2发生取代反应得到
,再与SOCl2发生取代反应得到![]() ,最后与NH(CH3)2反应得到
,最后与NH(CH3)2反应得到![]() ,合成路线流程图为
,合成路线流程图为
 。
。


科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2![]() 2NH3的能量变化图所示,该反应的热化学方程式是( )
2NH3的能量变化图所示,该反应的热化学方程式是( )
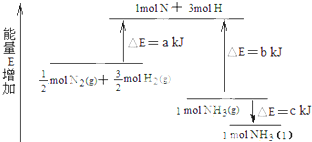
A.N2(g)+3H2(g)![]() 2NH3(l)△H=2(a-b-c) kJ/mol
2NH3(l)△H=2(a-b-c) kJ/mol
B.N2(g)+3H2(g)![]() 2NH3(l)△H=2(b-a) kJ/mol
2NH3(l)△H=2(b-a) kJ/mol
C.![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g)![]() NH3(l)△H=(b+c-a) kJ/mol
NH3(l)△H=(b+c-a) kJ/mol
D.![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)△H=(a+b)kJ/mol
NH3(g)△H=(a+b)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g)达到平衡,下列说法正确的是
CH3OH(g)达到平衡,下列说法正确的是
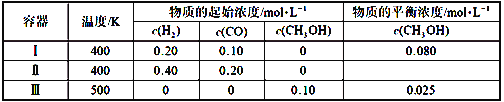
A. 该反应的正反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个恒容体积均为2.0L的容器中发生反应:PCl5(g) ![]() PCl3(g)+Cl2(g),下列说法正确的是( )
PCl3(g)+Cl2(g),下列说法正确的是( )
编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡 所需时间/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
A. 平衡常数K:容器Ⅱ>容器Ⅲ
B. 反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C. 反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 molL-1s-1
D. 容器Ⅲ中平衡后,等温条件下充入一定量He,平衡不发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3 + S ![]() Na2S2O3,常温下溶液中析出晶体为Na2S2O35H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如下图所示。
Na2S2O3,常温下溶液中析出晶体为Na2S2O35H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如下图所示。
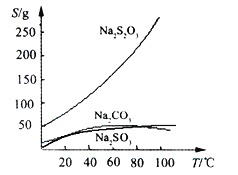

Ⅰ.现按如下方法制备Na2S2O35H2O:
将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按下图安装好装置。
(1)仪器2的名称为_________________,装置6中可放入_____________________(填字母)。
A.BaCl2溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.NaOH溶液
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二氧化硫气体较均匀的通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,反应原理为:
①Na2CO3+SO2 =Na2SO3+CO2 ②Na2S+SO2+H2O=Na2SO3+H2S
③2H2S+SO2=3S↓+2H2O ④Na2SO3+S![]() Na2S2O3
Na2S2O3
总反应为:2Na2S+Na2CO3+4SO2= 3Na2S2O3+CO2
随着二氧化硫气体的通入,看到溶液中有大量浅黄色固体析出,继续通二氧化硫气体,反应约半小时。当溶液中pH接近或不小于7时,即可停止通气和加热。溶液pH要控制不小于7理由是____________________________________(用离子方程式表示)。
Ⅱ.分离Na2S2O35H2O并标定溶液的浓度:

(3)为减少产品的损失,操作①为__________,操作②是抽滤洗涤干燥,其中洗涤操作是用_______(填试剂)作洗涤剂。
(4)蒸发浓缩滤液直至溶液呈微黄色浑浊为止,蒸发时为什么要控制温度不宜过高______________________________。
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量294g/mol)0.5880克。平均分成3份分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-, 三次消耗Na2S2O3溶液的平均体积为20.00mL,则所标定的硫代酸钠溶液的浓度为_______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓盐酸与二氧化锰固体加热反应来制备氯气(MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O),某兴趣小组制取氯气并进行氯气的性质实验装置如图,请回答下列问题:
MnCl2+Cl2↑+2H2O),某兴趣小组制取氯气并进行氯气的性质实验装置如图,请回答下列问题: 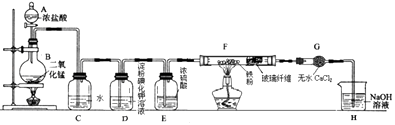
(1)仪器A的名称是 .
(2)C中反应的化学方程式为 , 所得溶液除水分子外,还含有的分子和离子中正确的是 .
A.Cl2、HCl、HClO,H+、Cl﹣ B.Cl2、Mn2+、HClO,H+、Cl﹣
C.Cl2、HClO,H+、Cl﹣、ClO﹣ D.Cl2、HCl、HClO,H+、Mn2+
(3)实验中观察到D溶液变蓝色,查资料得知淀粉碘化钾溶液是淀粉和碘化钾(KI)的混合溶液,碘单质(I2)遇淀粉显蓝色,且氯气可以从KI中置换出碘单质,写出该反应的化学方程式为 .
(4)F中氯气与铁粉反应制备无水三氯化铁,查资料知该化合物呈棕红色、易吸水潮解,100℃左右时升华.E中浓硫酸的作用是 , 双通管F中玻璃纤维(不参与反应)的作用是 .
(5)H中盛有NaOH溶液,其作用是 , 发生反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与盐类水解无关的是
A.金属焊接时可用NH4Cl溶液作除锈剂 B.配制FeSO4溶液时,加入一定量Fe粉
C.长期施用铵态氮肥会使土壤酸化D.使用泡沫灭火器灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用元素周期律解释的是
A. Mg、Al与同浓度盐酸反应,Mg更剧烈 B. 向Na2SO3溶液中加盐酸,有气泡产生
C. 0.1 mol·L-1 溶液的碱性:MaOH>LiOH D. 气态氢化物的稳定性:HBr>HI
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com