
科目: 来源:不详 题型:填空题

| | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
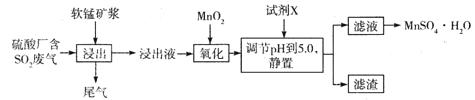

查看答案和解析>>
科目: 来源:不详 题型:填空题
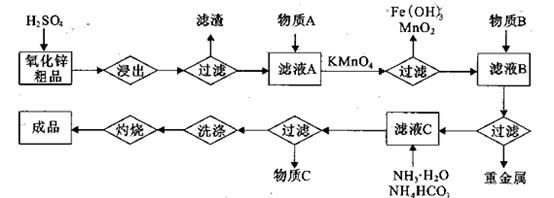
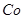 +、Mn2+等
+、Mn2+等| A.NH3.H2O | B.Na2CO3 | C.H2SO4 | D.ZnO |
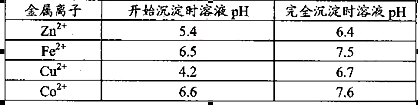
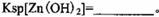 。
。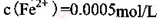 ,则处理1
,则处理1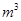 该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。
该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。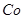 2+可利用置换反应除去,则物质B是_________。
2+可利用置换反应除去,则物质B是_________。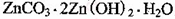 ,生成该沉淀的化学方程式为________。
,生成该沉淀的化学方程式为________。查看答案和解析>>
科目: 来源:不详 题型:单选题
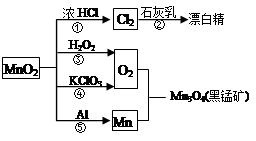
| A.反应①②③④⑤均属于氧化反应和离子反应 |
| B.反应⑤说明该条件下铝的还原性强于锰 |
| C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1 |
| D.反应①中氧化剂与还原剂的物质的量之比为1:4 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
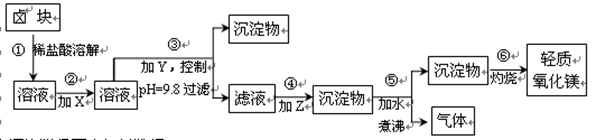
| 表1: 生成氢氧化物沉淀的pH | 表2: 原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
| Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
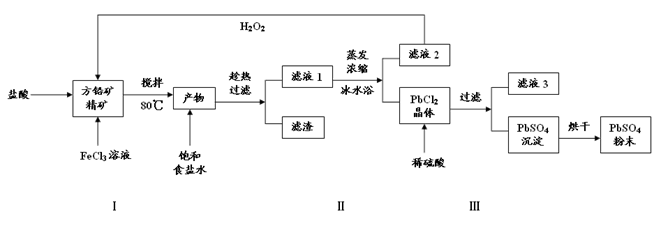
 PbCl4-(aq) △H>0
PbCl4-(aq) △H>0查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.由水电离产生的c(H+)=1×10-2mol?L-1溶液中,可能存在:CO32-、NH4+、Cl-,Na+ |
| B.某醋酸稀溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| C.Ba(OH)2溶液中加人过量的Al2(SO4)3溶液,其离子方程式为:3Ba2++60H-+2Al3++3SO42-=3BaS04↓+2Al(0H)3↓ |
| D.物质的量浓度均为1mol?L-1的NaCl和MgCl2混合液中,含有Cl-的数目为3NA(NA表示阿伏加德罗常数的值) |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.pH=12的澄清的溶液中:K+、Na+、MnO4-、SO42- |
| B.c(Al3+)=0.1mol?L-1的溶液中:Na+、Cl-、HCO3-、SO42- |
| C.甲基橙呈红色的溶液中:NH4+、Ba2+、AlO2-、Cl- |
| D.加入少量铝粉后能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.K+、Na+、AlO2-、NO3- | B.Al3+、Mg2+、SO42-、Cl- |
| C.Fe2+、NO3-、Cl-、SO42- | D.Fe3+、I-、ClO-、Na+ |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.Na+、CO32-、Ca2+、NO3- | B.Na+、NO3-、Al3+、Cl- |
| C.K+、SO42-、Cl-、Cu2+ | D.Ba2+、Cl-、K+、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com