
科目: 来源:不详 题型:单选题
| A.工业上利用N2和H2合成氨,实现人工固氮 |
| B.实验室用NH4Cl和Ca(OH)2制备NH3 |
| C.用FeCl3溶液作为“腐蚀液”刻蚀电路铜板 |
| D.用Na2O2作潜水艇的供氧剂 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 该反应中,____________元素被还原;该反应中氧化剂和还原剂物质的量之比为__________。
该反应中,____________元素被还原;该反应中氧化剂和还原剂物质的量之比为__________。查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.2F2+2H2O=4HF+O2↑ | B.C+H2O CO+H2 CO+H2 |
| C.2Na+2H2O=2NaOH+H2↑ | D.3NO2+H2O=2HNO3+NO |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.Na2S水溶液在空气中变浑浊 |
| B.生活中使用明矾净水,除去水中的悬浮颗粒 |
| C.溶有二氧化氮的浓硝酸做火箭的助燃剂 |
| D.漂白粉漂白有色布条 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

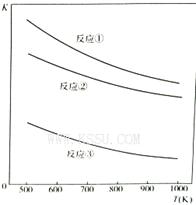
| A.反应①、②、③中铁的氧化物都是氧化剂 |
| B.反应①、②、③的正反应都是放热反应 |
| C.反应①、②、③中,温度越高H2S的的脱除率越高 |
| D.反应①、②、③中,压强越大H2S脱除率越高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com