
科目: 来源:不详 题型:单选题
| A.要配制100 mL 1 mol·L-1 NaOH溶液,需在白纸上称4 g NaOH固体,并且称量速度较慢 |
| B.称量时托盘天平的砝码已被锈蚀 |
| C.溶解或稀释溶质时烧杯尚未干燥 |
| D.定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.将NA个HCl分子溶于500 mL水中得到2.0 mol·L-1的盐酸 |
| B.在加热条件下,100 mL 18.4 mol·L-1的浓硫酸与足量金属铜反应得到的SO2的分子数为0.92NA |
| C.密闭容器中,1 mol SO2与0.5 mol O2充分反应,转移的电子数小于2NA |
| D.用惰性电极电解AgNO3溶液,产生11.2 L O2时,转移2 mol电子 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
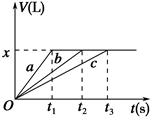
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
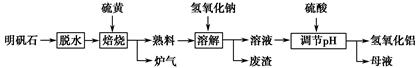
 Al2(SO4)3+
Al2(SO4)3+ S
S
 Al2O3+
Al2O3+ ______↑。
______↑。查看答案和解析>>
科目: 来源:不详 题型:填空题
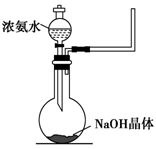
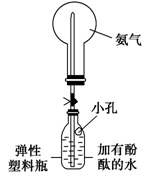
 NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动
NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动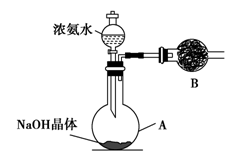
查看答案和解析>>
科目: 来源:不详 题型:填空题
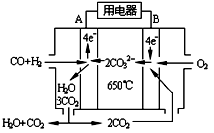
 4FeO+CO2↑。
4FeO+CO2↑。查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.1 mol Cl2发生反应时,转移的电子数一定是2NA |
| B.标准状况下,22.4L H2O中所含氢原子数目为2NA |
| C.1.0 L的 0.1 mol·L-1Na2CO3溶液中含有的CO32-数目为0.1NA |
| D.7.8 g 过氧化钠(Na2O2)固体中阴、阳离子总数为0.3NA |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.1molC2H6中共价键数为8NA |
| B.3.2 g O2和O 3的混合气中氧原子数为0.2NA |
| C.1L 0.1mol·L-1Al2(SO4)3溶液中Al3+数为0.2NA |
| D.标准状况下,22.4 L甲醇的分子数为NA |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.25℃时,pH=12的 Ba(OH)2溶液中含有的OH-数目为0.01 NA |
| B.9 g H218O含有的中子数为5NA |
| C.常温常压下,28 g C2H4、C3H6的混合气体中含有碳原子的数目为2NA |
| D.分子数为NA的CO、N2混合气体体积约为22.4L,质量为28g |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 (4)含铬化合物有毒,对人畜危害很大.因此含铬废水必须进行处理才能排放.
(4)含铬化合物有毒,对人畜危害很大.因此含铬废水必须进行处理才能排放.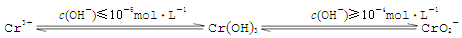
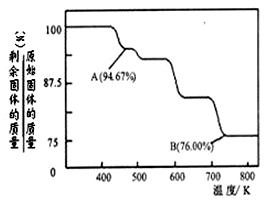
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com