
科目: 来源:不详 题型:单选题
| A.在周期表中金属与非金属的分界处可以找半导体材料 |
| B.H2S、H2Se、HF的热稳定性依次增强 |
| C.NaOH、KOH、Mg(OH)2的碱性依次减弱 |
| D.Cl、S、N元素的非金属性依次增强 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为白色固体,HAt不稳定,AgAt感光性很强 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)无色、有毒,比H2S更不稳定 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.元素非金属性由弱到强的顺序为Z<Y<X |
| B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C.三种元素的气态氢化物中,Z的气态氢化物最稳定 |
| D.原子半径由大到小的顺序为Z<Y<X |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| A.①②③ | B.②④⑤ | C.②③④ | D.①②④⑤ |
查看答案和解析>>
科目: 来源:不详 题型:填空题
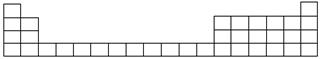
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | | | | | | | ② |
| 2 | | | | ③ | ④ | ⑤ | ⑥ | |
| 3 | ⑦ | ⑧ | | | | ⑨ | ⑩ | |
查看答案和解析>>
科目: 来源:不详 题型:单选题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 元素代号 | 原子半径/nm | 主要化合价 |
| X | 0.160 | +2 |
| Y | 0.143 | +3 |
| Z | 0.102 | +6、-2 |
| L | 0.099 | +7、-1 |
| M | 0.077 | +4、-4 |
| Q | 0.074 | -2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.①②③ | B.①③④ | C.②③④ | D.①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com