
科目: 来源:不详 题型:单选题
| A.元素的种类由核外电子数决定 |
| B.原子的种类由原子核内质子数与中子数共同决定 |
| C.核外电子排布相同的两个原子一定是同种原子 |
| D.某元素的原子核内有m 个质子,n 个中子,则该元素的相对原子质量为m + n |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.CH4>NH3>H2O>HF | B.SiH4>NH3>H2S>HCl |
| C.HF>H2O>NH3>PH3 | D.NH3>PH3>H2S>HBr |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.锑元素的质量与12C原子质量1/12的比值 |
| B.一个锑原子的质量与12C原子质量1/12的比值 |
C.按各种锑的天 然同位素的相对原子质量与这些同位素所占的一定百分比计算出的平均值 然同位素的相对原子质量与这些同位素所占的一定百分比计算出的平均值 |
| D.按各种锑的天然同位素质量数与这些同位素所占的一定百分比计算出的平均值 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 、
、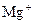 、
、 、
、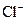 、
、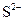 等五种离子按半径由大到小的顺序排列(用离子符号表示)____________________。
等五种离子按半径由大到小的顺序排列(用离子符号表示)____________________。查看答案和解析>>
科目: 来源:不详 题型:填空题
 试回答:
试回答:查看答案和解析>>
科目: 来源:不详 题型:单选题

查看答案和解析>>
科目: 来源:不详 题型:填空题
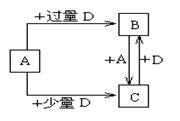
查看答案和解析>>
科目: 来源:不详 题型:填空题
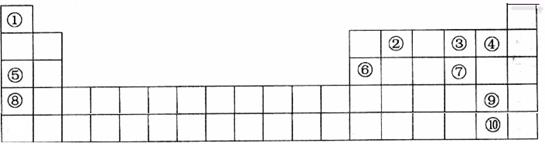
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 元素 | 信息 |
| A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | B原子得一个电子后2p轨道全满 |
| C | C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大 |
| D | D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于其中子数 |
| E | E+和B- 具有相同的电子层结构 具有相同的电子层结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com