
科目: 来源:不详 题型:单选题
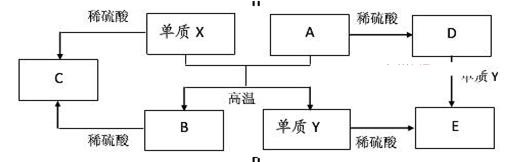
 Fe2O3 + 2Al
Fe2O3 + 2Al 查看答案和解析>>
科目: 来源:不详 题型:填空题
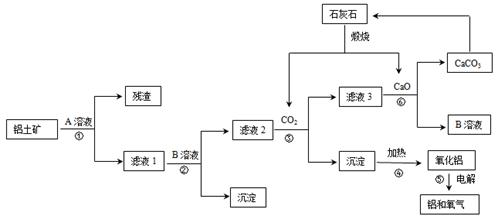

查看答案和解析>>
科目: 来源:不详 题型:填空题
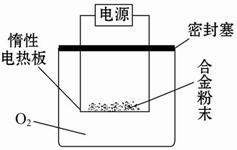
 4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
查看答案和解析>>
科目: 来源:不详 题型:实验题
 测定剩余固体质量,实验中发生反应的化学方程式是_________________________。
测定剩余固体质量,实验中发生反应的化学方程式是_________________________。 测定生成气体的体积实验装置:
测定生成气体的体积实验装置: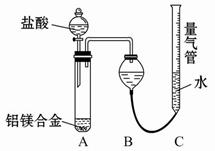
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:填空题
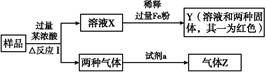
查看答案和解析>>
科目: 来源:不详 题型:填空题
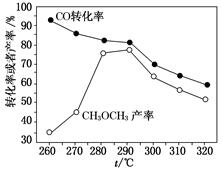
查看答案和解析>>
科目: 来源:不详 题型:单选题
 4AlCl3(g)+3O2(g) ΔH>0 。下列分析错误的是( )
4AlCl3(g)+3O2(g) ΔH>0 。下列分析错误的是( )| A.增大反应体系的压强,反应速率可能加快 |
| B.加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量 |
| C.电解熔融的Al2O3和AlCl3溶液均能得到单质铝 |
| D.将AlCl3·6H2O在氯化氢气流中加热,也可制得无水氯化铝 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.MgO、Al2O3、SiO2分别是碱性氧化物、两性氧化物和酸性氧化物 |
| B.三者均可以采用单质在空气中燃烧或加热的方法制得 |
| C.MgO和Al2O3可以作为耐高温材料,SiO2可用于制作光导纤维 |
| D.分别电解熔融状态的MgO、Al2O3、SiO2可以制得Mg、Al、Si |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com