
科目: 来源:不详 题型:单选题
| A.用盐酸可以洗去铜表面的铜锈 |
| B.向氯化铁溶液中加入适量氧化铜固体,可得到红褐色沉淀 |
| C.0.1mol/L的CuSO4溶液中,Cu2+的微粒数目一定小于0.1NA(设NA为阿伏伽德罗常数) |
| D.在FeSO4溶液中加入CuS固体,溶液中c(Fe2+)不变,说明Ksp(CuS)远小于Ksp(FeS) |
查看答案和解析>>
科目: 来源:不详 题型:实验题
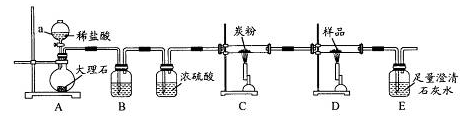
查看答案和解析>>
科目: 来源:不详 题型:填空题
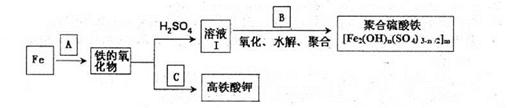


查看答案和解析>>
科目: 来源:不详 题型:实验题
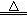 2KNO2+O2↑ Fe(NO3)2
2KNO2+O2↑ Fe(NO3)2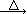 FexOy+NO2↑+O2↑
FexOy+NO2↑+O2↑| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量Fe(NO3)2固体于试管中,加热分解。 | ,说明分解产生的气体中含有NO2。 |
| 步骤2:将产生的气体依次通过盛有足量 、浓硫酸的洗气瓶, 在最后一个出口检验。 | ,说明分解产生的气体中含O2。 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
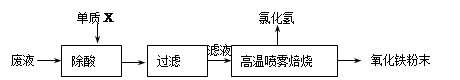
| 操作步骤 | 预期现象和结论 |
| 步骤1.取少量样品于试管中,_________________ ____________________________________________ | ___________________________ |
| 步骤2. ____________________________________________ | ___________________________ |
查看答案和解析>>
科目: 来源:不详 题型:填空题
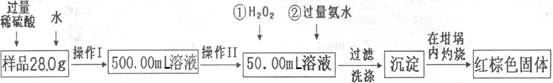
| A.50mL量筒 | B.100mL量筒 |
| C.50mL酸式滴定管 | D.50mL碱式滴定管 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.金属与盐溶液间的反应一定是置换反应 |
| B.能与酸反应的氧化物一定是碱性氧化物 |
| C.1 1H2和2 1H2的物理性质略有差异,化学性质几乎完全相同 |
| D.常见金属铁和铝在工业上是由热还原法制得的 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
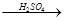 H2
H2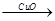 Cu ②CuO
Cu ②CuO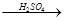 CuSO4
CuSO4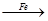 Cu
Cu| A.①多 | B.②多 | C.相等 | D.无法判断 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题
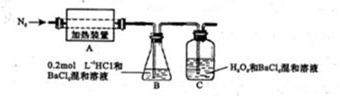
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com