
科目: 来源:不详 题型:单选题
| A.金属钠投入Ca(HCO3)2溶液,反应后有白色沉淀析出 |
| B.干粉灭火器能用于扑灭金属钠、钾的着火 |
| C.生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl |
| D.取用金属钠、钾时,所需实验用品有小刀、镊子、滤纸、玻璃片 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.CaO2中阴、阳离子的个数比为1:1 |
| B.CaO2对面粉增白原理与SO2漂白原理相似 |
| C.CaO2和水反应时,每产生1 molO2转移电子4 mol |
| D.CaO2放入NaHCO3溶液中,会放出二氧化碳,并产生白色浑浊 |
查看答案和解析>>
科目: 来源:不详 题型:填空题

 ,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为________。
,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为________。
查看答案和解析>>
科目: 来源:不详 题型:实验题
| 实验操作 | 预期现象和结论 |
| 取少量反应后固体于试管中, 。 | |
查看答案和解析>>
科目: 来源:不详 题型:填空题
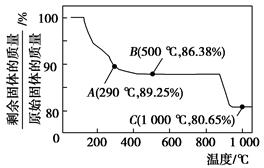
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.金属在地壳中的丰度 |
| B.金属在自然界中的存在形式 |
| C.金属的还原性强弱 |
| D.金属的利用价值 |
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:单选题
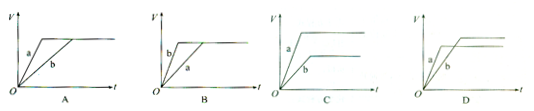
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com