
科目: 来源:不详 题型:单选题
| A.浓H2SO4具有吸水性,因而使蔗糖碳化 |
| B.浓H2SO4在常温下可迅速与铜片反应放出SO2气体 |
| C.浓H2SO4是一种干燥剂,能够干燥氨气、氢气等气体 |
| D.浓H2SO4在常温下能够使铁、铝钝化 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.SO2有漂白性,所以能使品红溶液、溴水、KMnO4溶液褪色 |
| B.二氧化硫的水溶液能使紫色石蕊溶液变红,说明它能与水反应生成H2SO3 |
| C.实验室可用氢氧化钠溶液处理含有二氧化硫的尾气 |
| D.将等物质的量的Cl2和SO2同时通入品红溶液中,品红溶液不褪色 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.浓硫酸具有脱水性 | B.浓硫酸具有吸水性 |
| C.浓硫酸稀释放热 | D.气体在水中的溶解度随温度升高而减小 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.大于0.90mol | B.等于0.45mol |
| C.在0.45mol和0.90mol之间 | D.小于0.45mol |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.一定条件下弱酸可以制强酸 | B.饱和溶液中H2S比CuS提供的S2-浓度大 |
| C.CuS不溶于硫酸 | D.反应FeSO4+H2S ® FeS¯+H2SO4也能发生 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
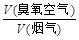 流量比为y,请通过计算列出y与x的关系式。
流量比为y,请通过计算列出y与x的关系式。查看答案和解析>>
科目: 来源:不详 题型:实验题
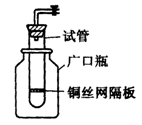
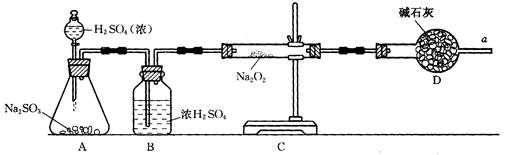
| A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧. |
| B.将C装置中反应后的固体物质溶于适量水配成溶液. |
| C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成. |
| D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.S的还原性 | B.S的漂白性 | C.SO2的还原性 | D.SO2的漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com