
科目: 来源:不详 题型:填空题
 Si(粗)+2CO↑,SiO2+3C
Si(粗)+2CO↑,SiO2+3C SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。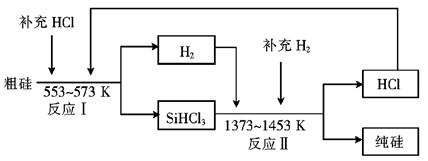
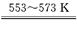 SiHCl3+H2,
SiHCl3+H2,查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.单质硅常用作半导体和光导纤维材料 |
| B.硅在自然界中只以化合态的形式存在 |
| C.SiO2与纯碱高温生成CO2,说明硅酸的酸性比碳酸强 |
| D.SiO2是非金属氧化物,它不与任何酸反应 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
 CH3OH(g)△H1=-116 kJ·mol-1
CH3OH(g)△H1=-116 kJ·mol-1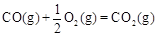 △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1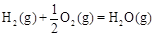 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1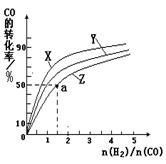
 CH3OH(g)的平衡常数K= 。
CH3OH(g)的平衡常数K= 。 | | 0min | 5min | 10min |
| CO | 0.1 | | 0.05 |
| H2 | 0.2 | | 0.2 |
| CH3OH | 0 | 0.04 | 0.05 |
查看答案和解析>>
科目: 来源:不详 题型:计算题
 CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。
CO(g)+H2(g) △H=+131.3kJ/mol,达到平衡后,体积不变时,能提高H2O的平衡转化率的措施是 。| A.升高温度 | B.增加碳的用量 |
| C.加入催化剂 | D.用CO吸收剂除去CO |
 CO2(g)+H2(g)得到如下数据:
CO2(g)+H2(g)得到如下数据:| 温度/℃ | 起始浓度mol/L | 平衡浓度mol/L | |
| CO(g) | H2O(g) | H2(g) | |
| 900 | 2.0 | 0.8 | 0.4 |
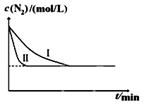
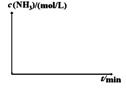
查看答案和解析>>
科目: 来源:不详 题型:推断题
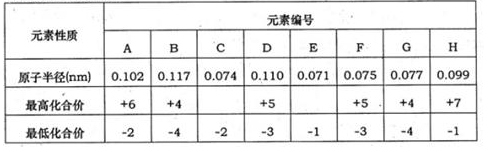

查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.光导纤维的主要成分是二氧化硅 | B.二氧化硅可以和水直接反应来制取硅酸 |
| C.硅可用作太阳能电池 | D.硅酸钠是制备硅胶和木材防火剂等的原料 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
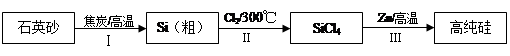
 Si(s) + 2ZnCl2(l) ΔH1 <0
Si(s) + 2ZnCl2(l) ΔH1 <0  Si(s) + 2ZnCl2(g) ΔH2 <0
Si(s) + 2ZnCl2(g) ΔH2 <0  Si(s) + 2ZnCl2(g) ΔH3 <0
Si(s) + 2ZnCl2(g) ΔH3 <0 查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.H2CO3比H2SiO3受热易分解 |
B.高温下能发生反应Na2CO3+SiO2 Na2SiO3+CO2↑ Na2SiO3+CO2↑ |
| C.CO2能溶于水生成碳酸,而SiO2却不溶于水 |
| D.CO2通入Na2SiO3溶液中有胶状沉淀生成 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
 Si3N4 +12HCl
Si3N4 +12HCl查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com