
科目: 来源:不详 题型:单选题
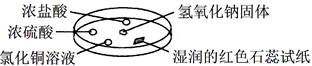
| 选项 | 实 验 现 象 | 解 释 |
| A | 浓盐酸附近产生白烟 | NH3与HCl反应生成了NH4Cl固体 |
| B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
| C | 氯化铜溶液变白色浑浊 | 白色浑浊的成分是Cu(OH)2 |
| D | 湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
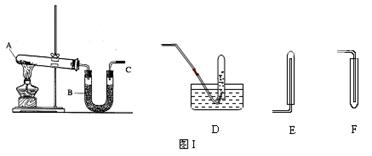
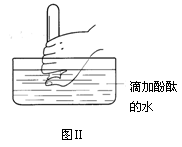
查看答案和解析>>
科目: 来源:不详 题型:实验题
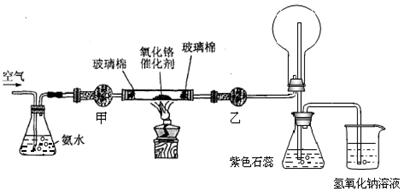
查看答案和解析>>
科目: 来源:不详 题型:实验题
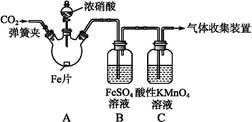
 Fe(NO)SO4(棕色) ΔH<0。
Fe(NO)SO4(棕色) ΔH<0。| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹。 | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 | 无明显现象。 |
| 加热烧瓶,反应开始后停止加热。 | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅;B中溶液变棕色;C中溶液紫色变浅。 ②反应停止后,A中无固体剩余。 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.浓硝酸和稀硝酸都具有氧化性 |
| B.铜与硝酸的反应属于置换反应 |
| C.金属与HNO3反应一般不产生氢气 |
| D.可用铁或铝制品盛装浓硝酸 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

| A.合金的熔点比其成分金属低,通常比成分金属具有更优良的金属特性 |
| B.铜银都能与稀硝酸反应,收集到的V L气体全为NO |
| C.操作Ⅰ是过滤,操作Ⅱ是洗涤,操作Ⅲ应是烘干 |
| D.根据反应收集到的气体体积可以计算铜和银的质量分数 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
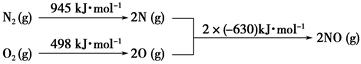
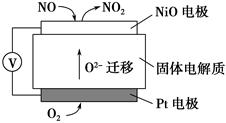
查看答案和解析>>
科目: 来源:不详 题型:实验题
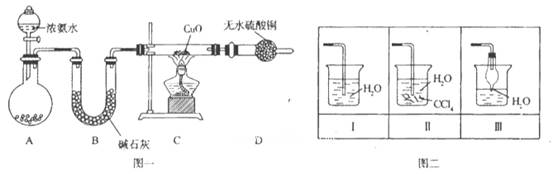
查看答案和解析>>
科目: 来源:不详 题型:填空题
 N2O4(g) △H <0;N2O4为无色气体。
N2O4(g) △H <0;N2O4为无色气体。 | 实验步骤 | 实验现象 | 实验结论 |
| ①分别用两支注射器收集NO2,并将注射器针头插入橡皮塞中以封口。 ②_____________________ _______________________ ________________________ _______________________ ________________________ | _______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ | _______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ |
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com